Diverse-alb și roșu-apar leziuni ale mucoasei bucale, inclusiv leucoplazie, erythroplakia, candidoza, limba geografică, lichen plan, lichenoid leziuni, și altele. Leucoplazia orală și eritroplazia orală sunt bine cunoscute a fi leziuni precanceroase, în timp ce potențialul malign al lichenului planus oral (OLP) și/sau leziunilor oralichenoide (OLLs) a fost subiectul multor discuții în ultimele decenii., Deoarece caracteristicile clinice și histologice ale acestor leziuni albe și roșii sunt similare, diagnosticul diferențial al acestora este important. Oral lichenul plan are o caracteristic bilaterale de distribuție, de obicei, implică mucoasa bucală, dorsală și ventrală suprafețe ale limbii și/sau a gingiei, atunci când se prezintă de multe ori ca desquamative gingivita.1,2 implicarea palatală și labială este neobișnuită. Este adesea asimptomatic, deși atunci când există zone de ulcerație, pacientul prezintă diferite grade de disconfort, exacerbate prin consumul de alimente picante sau acide.,
Există multe antigen-specifice mecanisme pot fi implicate în patogeneza OLP, inclusiv MHC I și MHC clasa a II-a limitat prezentării antigenului de lezionale keratinocite, activarea antigen-specifice CD4+ helper, celule T și T citotoxice CD8+-celule, expansiunea clonală de antigen celulele T specifice, și de keratinocite apoptotice declanșată de antigen-specifice citotoxice CD8+ T-celule.,roteins (HSPs), specii reactive de oxigen (ROS), stres, mastocitare chemotaxie și degranularea stimulată de celule T RANTES, celule endoteliale de adeziune molecula de exprimare stimulată de celule catarg TNF-a, T-celule MMP-9 activarea de celule catarg chymase, epitelială a membranei bazale perturbare de celule catarg proteaze sau T-celule MMP-9, factorul de apoptoza declanșată de epitelială a membranei bazale perturbare, intra-epiteliale CD8+ T-migrarea celulelor prin intermediul membranei bazale pauze, celulare inflamatorii supraviețuire prelungită de celule T RANTES și non-specifice T-celule de recrutare de către keratinocite derivate chemokine.,5,6


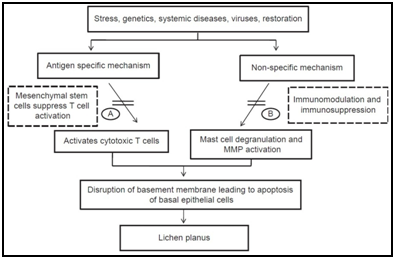
Figura 5 Diferite etiopatogenic căile propuse pentru lichen plan oral bazate pe diferite studii.OLP poate fi împărțit în șase tipuri (reticulare, papule, plăci, atrofice, erozive și buloase) sau două tipuri, alb și roșu, în timp ce este cel mai frecvent clasificat în trei tipuri, reticular, atrofic și eroziv. Leziunile nu sunt omogene și unele cazuri se pot prezenta ca un amestec al acestor subtipuri clinice., Organizația Mondială a Sănătății (OMS) a elaborat un set de criterii de diagnostic pentru OLP în 1978, care a fost revizuit în 2003. Criteriile de diagnostic OMS modificate implică diferențierea între OLP și OLLs.7,8 în aceste criterii modificate ale OMS, caracteristica clinică esențială a OLP este definită a fi prezența leziunilor bilaterale care prezintă o rețea de linii albe(model reticular), dar nu a leziunilor plăcii, atrofice, erozive și buloase. Atunci când leziunea reticulară bilaterală este absentă, atunci este desemnată ca fiind „compatibilă clinic cu OLP”.,biopsia și examinarea histopatologică a țesutului afectat pot fi necesare pentru a exclude alte boli care pot imita lichenul plan oral , de exemplu lupusul eritematos discoid și pentru a identifica posibila displazie epitelială. Necesitatea biopsiei în toate cazurile de lichen planus suspectat este dezbătută, dar ar fi adecvată în cazurile atipice în prezentare, atrofice sau ulcerative. Testarea pielii pentru alergie la amalgam de mercur poate fi efectuată în cazul în care există suspiciunea că poate exista o reacție lichenoidă ca răspuns la acest material dentar., Cu toate acestea, există dezbateri cu privire la valoarea unei astfel de anchete. Histopatologic al OLP a fost descris pentru prima data de Dubreuill în 1906, iar în 1972, acesta a fost revizuit de către Shklar care a descris trei caracteristici: acoperitoare de keratinizare, lichefiere degenerarea bazal strat de celule și un dens subepitelial trupa de limfocite.una dintre cele mai importante probleme legate de OLP este potențialul său de transformare malignă în OSCC., Deși OMS a clasificat OLP ca o afecțiune precanceroasă, riscul de transformare malignă a OLP rămâne un subiect de dezbatere în literatura de specialitate. Nu este sigur ce mecanisme ar putea provoca trans-formarea malignă a OLP. Preferențiale site-uri de Oral Squammous Carcinom cu Celule (OSCC) care se dezvoltă din OLP leziunile sunt limba și mucoasa bucală, iar incidența este mai mare în primul caz decât acesta din urmă, în timp ce displazia epitelială în OLP este mai răspândită în mucoasa bucală.,Scopul tratamentului lichenului planus oral simptomatic este de a vindeca zone cu ulcerații dureroase sau vezicule. Ar trebui adoptată o abordare treptată. Terapia cu corticosteroizi topici este pilonul principal al tratamentului pentru boala ulcerativă. Există dovezi limitate din studiile randomizate controlate cu privire la eficacitatea exactă a diferitelor preparate care sunt utilizate în mod obișnuit., Ca adjuvant la terapie, pacienții trebuie, de asemenea, avertizați cu privire la necesitatea menținerii unui standard ridicat de igienă orală și trebuie eliminate orice cauze ale traumatismelor mucoasei, cum ar fi protezele dentare necorespunzătoare, cuspidele ascuțite și restaurările dentare slabe. Pacienții trebuie informați că există un risc foarte mic de malignitate asociat cu lichen plan oral și că monitorizarea pe termen lung este adecvată.10
în cazul nostru, utilizarea metodică și sistematică a tacrolimusului (imunomodulator) a arătat o îmbunătățire drastică în vindecarea completă a leziunilor persistente., Tacrolimus este un inhibitor macrolidic al calcineurinei. Calcineurina este o serină/treonină proteică fosfatază dependentă de calciu și calmodulină care activează celulele T ale sistemului imunitar. Când are loc activarea receptorului celulei T, există o creștere a calciului intracelular care, în prezența calmodulinei ca catalizator, activează calcineurina. Această etapă este urmată de” de fosforilare ” care stimulează mișcarea factorului de transcripție al factorului Nuclear al celulelor T activate în nucleul celulei T, mărind astfel activitatea genelor care codifică IL-2 și alte citokine., S-a constatat că acesta este unul dintre mecanismele care duc la leziuni asemănătoare OLP. În acest mecanism al bolii, tacrolimusul acționează în faza de defosforilare (Figura 6), obstrucționând-o și determinând fosforilarea. În cele din urmă, aceasta scade activitatea genelor care codifică diferite ILs, ceea ce încetează progresul către leziuni asemănătoare OLP. Acest lucru a fost reprezentat pictorial mai jos.11,12
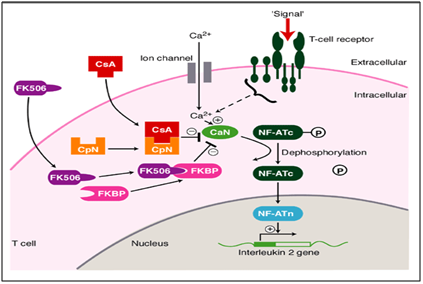
Figura 6 Mecanismul de acțiune al tacrolimus ca un imunomodulator în tratamentul oral erozive lichen plan.,diverse studii au constatat că tacrolimusul topic este eficace în tratamentul OLP și unele au raportat, de asemenea, un răspuns terapeutic inițial mai bun decât alte medicamente, inclusiv corticosteroizii. Dar studiile care evaluează eficacitatea tacrolimusului topic la populația indiană, în special pe perioade lungi, sunt rare. S-a raportat că Tacrolimus (0, 1% M/v) este eficace și sigur pentru tratamentul OLP de către diverși investigatori., S-a dovedit a fi un mijloc eficient de control al simptomelor și semnelor de lichen plan eroziv sau ulcerativ oral și nu a avut efecte adverse notabile pe o durată medie de aplicare de 19,8 luni.13 într-o meta analiză de Chamani G și colab.,14 S-a ajuns la concluzia că tacrolimusul topic este o alternativă eficientă la diferiți corticosteroizi și poate fi considerat ca terapie de primă linie în tratamentul OLEP.