diverses lésions blanches et rouges se produisent dans la muqueuse buccale, y compris la leucoplasie, l’érythroplasie, la candidose, la langue géographique, le lichen plan, les lésions La leucoplasie orale et l’érythroplasie orale sont bien connues pour être des lésions précancéreuses, tandis que le potentiel malin du lichen plan oral (OLP) et/ou des lésions orallichénoïdes (OLLs) a fait l’objet de nombreuses discussions au cours des dernières décennies., Étant donné que les caractéristiques cliniques et histologiques de ces lésions blanches et rouges sont similaires, le diagnostic différentiel d’entre elles est important. Le lichen plan Oral a une distribution bilatérale caractéristique, impliquant généralement la muqueuse buccale, les surfaces dorsale et ventrale de la langue et/ou de la gencive, alors qu’il se présente souvent comme une gingivite desquamative.1,2 l’atteinte Palatine et labiale est inhabituelle. Il est souvent asymptomatique, bien que lorsqu’il existe des zones d’ulcération, le patient éprouve divers degrés d’inconfort, exacerbés par la consommation d’aliments épicés ou acides.,
de nombreux mécanismes spécifiques à l’antigène peuvent être impliqués dans la pathogenèse de L’OLP, notamment la présentation restreinte de l’antigène de classe I et de classe II par les kératinocytes lésionnels, l’activation des lymphocytes T auxiliaires CD4+ spécifiques à l’antigène et des lymphocytes T cytotoxiques CD8+, l’expansion clonale des lymphocytes T spécifiques à l’antigène et l’apoptose des kératinocytes déclenchée par les lymphocytes T cytotoxiques CD8+ spécifiques à l’antigène.,rotéines (HSP), espèces réactives de l’oxygène (ROS), stress, chimiotaxie et dégranulation des mastocytes stimulées par les RANTES des lymphocytes T, expression de la molécule d’adhésion des cellules endothéliales stimulée par le TNF-a des mastocytes, activation des lymphocytes T MMP-9 par la chymase des mastocytes, perturbation de la membrane basale épithéliale par les protéases des mastocytes ou MMP-9 des lymphocytes T, apoptose des kératinocytes déclenchée par rantes and non-specific T-cell recruitment by keratinocyte-derived chemokines.,5,6


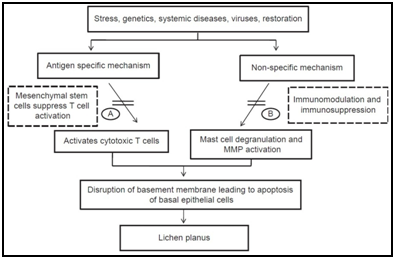
la Figure 5 Divers étiopathogéniques des voies proposées pour l’oral lichen plan s’appuyant sur différentes études.
L’OLP peut être divisé en six types (réticulaire, papule, plaque, atrophique, érosive et bulleuse), ou deux types, blanc et rouge, alors qu’il est le plus souvent classé en trois types, réticulaire, atrophique et érosif. Les lésions ne sont pas homogènes et certains cas peuvent se présenter comme un mélange de ces sous-types cliniques., L’Organisation Mondiale de la santé (OMS) a élaboré en 1978 un ensemble de critères diagnostiques pour les PLO qui a été révisé en 2003. Les critères de diagnostic modifiés de l’OMS impliquent une différenciation entre les OLP et les Oll.7,8 dans ces critères modifiés de l’OMS, la caractéristique clinique essentielle de la PLO est définie comme étant la présence de lésions bilatérales présentant un réseau de lignes blanches(motif réticulaire) ressemblant à une dentelle, mais pas de lésions de plaque, atrophiques, érosives et bulleuses. Lorsque la lésion réticulaire bilatérale est absente, elle est désignée comme « cliniquement compatible avec OLP ».,
une biopsie et un examen histopathologique des tissus affectés peuvent être nécessaires pour exclure d’autres maladies pouvant imiter le lichen plan buccal , par exemple le lupus érythémateux discoïde et pour identifier une éventuelle dysplasie épithéliale. La nécessité d’une biopsie dans tous les cas de suspicion de lichen plan est débattue mais elle serait appropriée dans les cas de présentation atypique, atrophique ou ulcéreuse. Des tests cutanés pour l’allergie à l’amalgame de mercure peuvent être entrepris lorsqu’il y a un soupçon qu’il peut y avoir une réaction lichénoïde en réponse à ce matériel dentaire., Cependant, la valeur d’une telle enquête fait l’objet d’un débat. L’histopathologie de L’OLP a été décrite pour la première fois par Dubreuill en 1906, et en 1972, elle a été révisée par Shklar qui a décrit trois caractéristiques: la kératinisation sus-jacente, la dégénérescence par liquéfaction de la couche basale des cellules et une bande dense sous-épithéliale de lymphocytes.
l’un des problèmes les plus importants concernant le PLO est son potentiel de transformation maligne en OSCC., Bien que l’OMS ait classé la PLO comme une condition précancéreuse, le risque de transformation maligne de la PLO reste un sujet de débat dans la littérature. On ne sait pas quels mécanismes pourraient causer la trans-formation maligne de L’OLP. Les sites préférentiels du carcinome Squammeux Oral (OSCC) qui se développe à partir de lésions OLP sont la langue et la muqueuse buccale, et l’incidence est plus élevée dans le premier que dans le second, tandis que la dysplasie épithéliale dans OLP est plus répandue dans la muqueuse buccale.,9
le traitement du lichen plan oral symptomatique vise à guérir les zones d’ulcération douloureuse ou de cloques. Une approche par étapes devrait être adoptée. La corticothérapie topique est le pilier du traitement de la maladie ulcéreuse. Les essais contrôlés randomisés ne fournissent que peu de preuves quant à l’efficacité précise des diverses préparations couramment utilisées., En complément du traitement, les patients doivent également être informés de la nécessité de maintenir un niveau élevé d’hygiène bucco-dentaire et toutes les causes de traumatisme de la muqueuse telles que des prothèses mal ajustées, des cuspides pointues et de mauvaises restaurations dentaires doivent être éliminées. Les Patients doivent être informés qu’il existe un très faible risque de malignité associé au lichen plan oral et qu’une surveillance à long terme est appropriée.10
dans notre cas, l’utilisation méthodique et systématique du Tacrolimus (immunomodulateur) a montré une amélioration drastique de la guérison complète des lésions persistantes., Le Tacrolimus est un inhibiteur de la calcineurine des macrolides. La calcineurine est une protéine phosphatase sérine/thréonine dépendante du calcium et de la calmoduline qui active les cellules T du système immunitaire. Lorsque l’activation du récepteur des lymphocytes T se produit, il y a augmentation du calcium intracellulaire qui, en présence de calmoduline en tant que catalyseur, active la calcineurine. Cette étape est suivie par la” dé phosphorylation » qui stimule le mouvement du facteur de Transcription du facteur nucléaire des lymphocytes T activés vers le noyau des lymphocytes T, augmentant ainsi l’activité des gènes codant pour L’IL-2 et d’autres cytokines., Cela s’est avéré être l’un des mécanismes entraînant des lésions de type OLP. Dans ce mécanisme de la maladie, le TACROLIMUS agit au stade de la déphosphorylation (Figure 6), l’obstruant ainsi et provoquant la phosphorylation. Cela diminue finalement l’activité des gènes codant pour divers ILs, ce qui cesse la progression vers des lésions de type OLP. Cela a été picturalement représenté ci-dessous.11,12
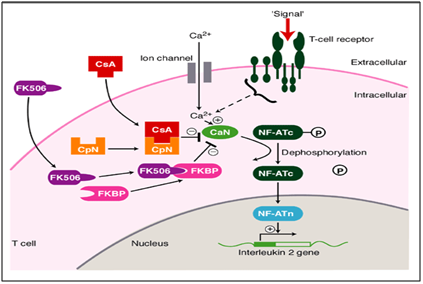
la Figure 6 Mécanisme d’action du tacrolimus comme un immunomodulateur dans le traitement de l’oral lichen plan érosif.,
diverses études ont révélé que le Tacrolimus topique était efficace dans le traitement de L’OLP et certaines ont également rapporté une meilleure réponse thérapeutique initiale que d’autres médicaments, y compris les corticostéroïdes. Mais les études évaluant l’efficacité du Tacrolimus topique dans la population indienne, en particulier sur de longues périodes, sont rares. Plusieurs chercheurs ont rapporté que le Tacrolimus (0,1% p/v) était efficace et sans danger pour le traitement de la PLO., Il s’est avéré être un moyen efficace de contrôler les symptômes et les signes du lichen plan buccal érosif ou ulcéreux et n’a eu aucun effet indésirable notable sur une durée moyenne d’application de 19,8 mois.13 dans une méta analyse de Chamani G et al.,14 Il a été conclu que le Tacrolimus topique est un substitut efficace à divers corticostéroïdes et peut être considéré comme un traitement de première intention dans la prise en charge de L’OLEP.