Eri valkoinen ja punainen leesioita esiintyy suun limakalvoilla, kuten leukoplakia, erythroplakia, kandidiaasi, karttakieli, lichen planus, lichenoidi vaurioita, ja muut. Oral leukoplakia ja suun erythroplakia ovat hyvin tiedossa olla syövän esiasteita, kun taas pahanlaatuinen mahdollisia suun punajäkälä (OLP) ja/tai orallichenoid vaurioita (L) on ollut paljon keskustelua viime vuosikymmeninä., Koska näiden valko-ja punaisten leesioiden kliiniset ja histologiset ominaisuudet ovat samanlaiset, niiden erotusdiagnoosi on tärkeä. Suun punajäkälä on luonteeltaan kahdenvälisiä jakelu, johon tavallisesti kuuluu posken limakalvolla, dorsum ja vatsa pinnat kielen ja/tai ikenen, kun se esitetään usein kuin desquamative ientulehdus.1,2 kuolemaan ja labial osallistuminen on epätavallista. Se on usein oireeton, vaikka kun on alueita, haavaumia, potilas kokee eriasteisia kipua, pahentaa syöminen mausteinen tai happamien elintarvikkeiden.,
On olemassa monia antigeeni-erityisiä mekanismeja voi olla mukana synnyssä OLP, kuten MHC luokan I ja MHC luokan II-rajoitettu antigeenin esittely lesional keratinosyyttien, aktivointi-antigeeni-erityinen CD4+ – auttaja-T-solujen ja CD8+ sytotoksisten T-solujen klonaalinen laajentaminen antigeeni-erityinen T-solut, ja keratinocyte apoptoosin laukaisi antigeeni-spesifisen CD8+ sytotoksiset T-solut.,roteins (HSPs), reaktiivisen hapen lajien (ROS), stressi, syöttösolujen kemotaksis ja fagosytoosia stimuloi T-solujen RANTES, endoteelin solujen kiinnittyminen molekyyli ilmaisun kannustanut maston solujen TNF-a, T-solujen MMP-9 aktivointi mast cell chymase, epiteelin tyvikalvon häiriöitä, joita syöttösolujen proteaasien tai T-solujen MMP-9, keratinocyte apoptoosin laukaisi epiteelin tyvikalvon häiriöitä, intra-epithelial CD8+ T-solujen vaeltamiseen läpi kellarissa kalvo hajoaa, tulehduksellisten solujen eloonjäämistä pitkäaikainen T-solu RANTES ja ei-spesifisten T-solujen rekrytointia keratinocyte-johdettu chemokines.,5,6


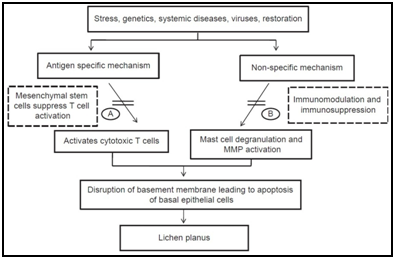
Kuva 5 Eri etiopathogenic reittejä ehdotti suun punajäkälä perustuvat erilaisiin tutkimuksiin.
OLP voi olla jaettu kuuteen ryhmään (reticular, papule, plakkia, atrofinen, erosive, ja rakkulainen tyypit), tai kaksi, valkoinen ja punainen, vaikka se on yleisimmin luokiteltu kolmeen ryhmään, reticular, atrofinen, ja erosive. Leesiot eivät ole homogeenisia, ja joissakin tapauksissa niitä voi esiintyä näiden kliinisten alatyyppien sekoituksena., Maailman terveysjärjestö WHO laati vuonna 1978 OLP: lle diagnostiset kriteerit, joita tarkistettiin vuonna 2003. Muutettu KUKA diagnostiset kriteerit liittyy erottelu OLP-ja L.7,8 näissä muutettu, KUKA perusteet, keskeiset kliiniset ominaisuus OLP on määritelty olevan läsnä kahdenvälisten vaurioita, että näyttely pitsi-kuin verkko valkoisia viivoja(reticular kuvio), mutta ei plakkia, atrofinen, erosive, ja rakkuloita. Kun kahdenvälisten reticular vaurio on poissa, niin, se on nimetty ”kliinisesti yhteensopiva OLP”.,
Biopsia ja histopatologisen tutkimuksen perusteella vaikuttaa kudoksen voi olla tarpeen sulkea pois muut sairaudet, jotka voivat jäljitellä suun punajäkälä , esimerkiksi discoid lupus erythematosus ja tunnistaa mahdollisia epiteelin dysplasia. Tarvitaan koepala kaikissa tapauksissa, joissa epäillään punajäkälä on keskusteltu, mutta se olisi tarkoituksenmukaista tapauksissa, jotka ovat epätyypillisiä esitys, atrofinen tai ulcerating. Iho testaus allergia elohopeaa amalgaamin voi olla suoritettava, jos on syytä epäillä, että siellä saattaa olla lichenoidi reaktio vastauksena tähän hammaslääkärin materiaalia., Tällaisen tutkinnan arvosta käydään kuitenkin keskustelua. Se histopatologinen tutkimus OLP oli ensimmäinen kuvattu Dubreuill vuonna 1906, ja vuonna 1972, se oli tarkistaa Shklar, jotka on kuvattu kolme ominaisuudet: päällä keratinisaatio -, nesteytys-rappeutumista tyvikerroksen ja tiheä epiteelinalaisella bändi lymfosyyttien.
Yksi tärkeimmistä asioista, jotka koskevat OLP on sen mahdollista muuttumista pahanlaatuinen OSCC., Vaikka, JOKA on luokiteltu OLP kuten syövän kunnossa, riski pahanlaatuisiin OLP on edelleen keskustelun kohteena kirjallisuudessa. On epävarmaa, mitkä mekanismit voivat aiheuttaa OLP: n pahanlaatuisen transmuodostuksen. Etuuskohteluun sivustoja Suun Squammous Cell Carcinoma (OSCC), joka kehittyy OLP vauriot ovat kielen ja posken limakalvolla, ja esiintyvyys on suurempi entisen kuin jälkimmäinen, kun epiteelin dysplasia OLP on yleisempää suun limakalvolta.,9
oireisen oraalisen jäkälän planuksen hoitotavoitteina on parantaa kivuliaiden haavaumien tai rakkuloiden alueita. Olisi omaksuttava vaiheittainen lähestymistapa. Ajankohtainen kortikosteroidihoito on ulseratiivisen sairauden hoidon tukipilari. On vain vähän näyttöä satunnaistetuissa, kontrolloiduissa tutkimuksissa, kuten tarkka tehoa eri valmisteita, jotka ovat yleisessä käytössä., Lisänä hoito, potilaille tulee myös kertoa, että on tarpeen säilyttää korkea suuhygienia ja mitään aiheuttaa limakalvon trauma, kuten huonosti istuva hammasproteesit, terävä nielut ja huono hampaiden restauraatiot, olisi poistettava. Potilaille tulee ilmoittaa, että on olemassa hyvin pieni riski maligniteetti liittyy suun punajäkälä ja että pitkän aikavälin seuranta on tarpeen.10
meidän tapauksessamme takrolimuusin (immunomodulaattori) järjestelmällinen ja järjestelmällinen käyttö paransi merkittävästi pysyviä leesioita kokonaan., Takrolimuusi on makrolidikalsineuriinin estäjä. Kalsineuriini on kalsium-ja kalmoduliiniriippuvainen seriini/treoniiniproteiinifosfataasi, joka aktivoi immuunijärjestelmän T-soluja. Kun aktivointi T-solujen reseptori ilmenee, on nousu solunsisäisen kalsiumia, joka läsnäollessa calmodulin katalysaattorina aktivoi kalsineuriini. Tämä vaihe seuraa ”de fosforylaation”, joka stimuloi liikkuvuutta Transcription factor Nuclear factor aktivoitu T-solujen tumaan T-solujen, mikä lisää toiminnan koodaavien geenien IL-2 ja muita sytokiineja., Tämän on todettu olevan yksi mekanismeista, jotka aiheuttavat OLP: n kaltaisia vaurioita. Tässä tautimekanismissa takrolimuusi vaikuttaa fosforylaatiovaiheessa (kuva 6), mikä estää sitä ja aikaansaa fosforylaation. Tämä lopulta vähentää eri ILs-geenejä koodaavien geenien aktiivisuutta, mikä lopettaa etenemisen kohti OLP: n kaltaisia leesioita. Tämä on kuvattu alla.11,12
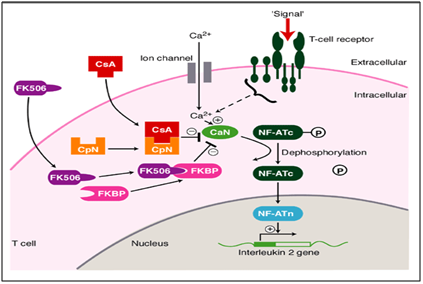
Kuva 6 vaikutusmekanismi takrolimuusi immunomodulaattorina hoitoon suun erosiivinen punajäkälä.,
Eri tutkimuksissa on havaittu, ajankohtainen Takrolimuusi olla tehokas hoito OLP ja joissakin on myös raportoitu paremman ensimmäisen hoitovasteen kuin muut lääkkeet, kuten kortikosteroidit. Tutkimukset paikallisen takrolimuusin tehon arvioimiseksi Intialaisväestössä erityisesti pitkinä ajanjaksoina ovat kuitenkin vähäisiä. Takrolimuusin (0,1% w/v) on todettu olevan tehokas ja turvallinen OLP: n hoidossa eri tutkijoiden toimesta., Se on todettu olevan tehokas keino valvoa oireita ja merkkejä erosive tai haavainen suun punajäkälä ja ei ollut merkittäviä haitallisia vaikutuksia yli keskimääräinen kesto sovellus 19,8 kuukautta.13 in a meta analysis by Chamani G et al.,14 todettiin, että paikallinen takrolimuusi on tehokas vaihtoehto erilaisille kortikosteroideille, ja sitä voidaan pitää OLEP-hoidon ensilinjan hoitona.