stål är det vanligaste materialet som används idag. Stål har emellertid en stor nackdel-dess höga korrosionshastighet. Skyddet av stålkonstruktioner och stålkomponenter är därför av stor ekonomisk betydelse.
det bästa korrosionsskyddet för stål erhålls med zink. Zinkbeläggningar på stål skyddar mot korrosion på två sätt:
- genom en barriäreffekt, dvs. de förhindrar att syre och fukt når stålytan.,
- genom att ge katodiskt skydd vid repor, chips, kanter etc.
zink är en metall med en relativt låg galvanisk potential och en hög tendens att korrodera. Korrosionshastigheten är emellertid låg i de flesta miljöer, eftersom beläggningens yta snabbt är täckt med korrosionsprodukter, som därefter skyddar mot ytterligare korrosion.
korrosion i atmosfären
När ett varmförzinkat föremål lämnar zinkbadet attackeras objektets yta omedelbart av syre i luften., Det resulterande oxidskiktet har mycket liten förmåga att skydda mot korrosion. Vatten och koldioxid i luften förändrar emellertid snabbt oxidskiktet till zinkkarbonater. Dessa ger ett förseglat lager med mycket god vidhäftning. Eftersom karbonaten har mycket låg löslighet i vatten ger de utmärkt skydd mot zinkbeläggningens yta. Den ursprungliga blanka ytan med metallisk lyster försvinner för att ersättas av matt, ljusgrå färg (fig.1).

bild 1., Exponerad yta av en zinkbeläggning med yttre skikt av ren zink. Den blanka ytan försvinner för att ersättas av grå korrosionsprodukter (ibland kallad zinkpatina).

Fig. 2. Missfärgad yta på belysningskolonnen. Beläggningen består huvudsakligen av en järn-zinklegering som sträcker sig till ytan. Järn utsätts under korrosion, vilket leder till rostbildning. Det är bara ytrost och är endast av estetisk betydelse.,
utomhusluft innehåller större eller mindre mängd frätande element — gaser, sot, fuktighet (dimma, dagg, regn, snö), inert och aggressivt damm. Nivåerna kan variera med plats och tid på året. Sulfater och sulfiter av zink är vattenlösliga och har dålig vidhäftning till zinkytan. De tvättas därför lätt bort av regn. En frisk zinkyta utsätts sedan för angrepp av syre i luften och korrosionscykeln upprepas. Korrosion i luft som innehåller svaveloxider är därför större än i ren luft., Mängden svaveldioxid i atmosfären har dock minskat drastiskt under de senaste åren, och därför har zinkkorrosionen också minskat.
i marina miljöer påverkas zinkkorrosionen av luftens salthalt. Marin luft innehåller emellertid små mängder magnesiumsalter, med goda passive influenser. Korrosion är därför inte så stor som kan förväntas. Salthalten i luften minskar snabbt bort från kusten.
zinkkorrosionen påverkas av många faktorer., Detta innebär att en allmänt tillämplig formel för korrosionshastigheter inte kan ges. Zinkbeläggningar har dock använts under lång tid, under ett brett spektrum av förhållanden, för att skydda stål mot rost. Ett stort antal långsiktiga tester har också genomförts. Kunskap om korrosion av zink och korrosionshastigheter i olika miljöer är därför bra. Idag finns det exempel på zinkbeläggningar som har exponerats i mer än hundra år.
färgen på korrosionsprodukter varierar beroende på den miljö där de bildas., Marina miljöer ger något vitare korrosionsprodukter jämfört med landsbygds-och stadsmiljöer. Korrosionsprodukter är vanligtvis mörkaste i stadsmiljöer.
korrosion i vätskor
zinkytan är i allmänhet täckt med ett skyddande skikt av korrosionsprodukter när den är nedsänkt i en vätska. Vätskor kan emellertid vara sura eller alkaliska och kan innehålla upplösta eller fasta partiklar av aggressiva ämnen. Vätskans temperatur och flödeshastighet är också av betydelse., Allt detta innebär att det skyddande skiktet kan ha en mycket varierande komposition eller kanske inte bildas alls.
elektrokemisk korrosion, som spelar en underordnad roll i luften, är av större betydelse i vätskor. Graden av elektrokemisk korrosion beror på vätskans elektriska ledningsförmåga, vilket påverkar zinkskiktets skyddande inflytande över större eller mindre områden.
vätskans pH-värde är av största betydelse. Zinkkorrosionshastigheten är normalt låg och stabil i pH-intervallet 5,5-12,5, vid temperaturer mellan 0 och 20 ° C., Korrosion utanför detta område är vanligtvis snabbare.
hårt vatten, som innehåller kalk och magnesium, är mindre aggressivt än mjukt vatten. Tillsammans med koldioxid bildar dessa ämnen sparsamt lösliga karbonater på zinkytan, vilket skyddar zinken mot ytterligare korrosion.
mjukt vatten angriper ofta zink, eftersom frånvaron av salter innebär att det skyddande skiktet inte kan bildas.
aggressivt mjukt vatten finns i många floder och sjöar i Finland, Norge, Sverige och liknande miljöer.
om flödet är större än 0.,5 m/s bildandet av det skyddande skiktet på zinkytan hämmas och korrosion accelererar.
vattentemperaturen är av stor betydelse för korrosionshastigheten. Över ca 55 ° C förvärvar de lagerbildande korrosionsprodukterna en grovkornig struktur och förlorar vidhäftning mot zinkytan. De lossnar lätt och exponerar ny, färsk zink för fortsatt och snabb korrosionsattack. Korrosionshastigheten når maximalt vid ca 70 °C, varefter den sjunker så att den vid 100 ° C är ungefär densamma som vid 50 °C.,
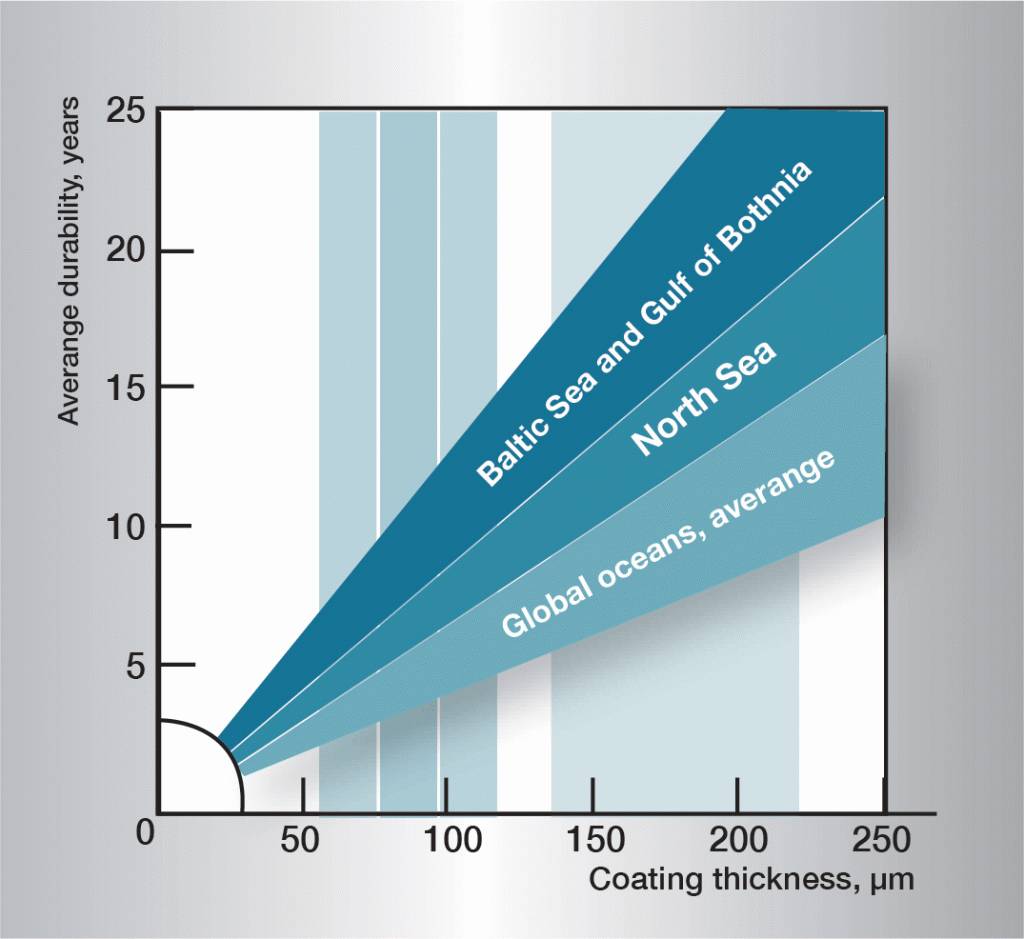
korrosionssekvensen i vatten är mycket komplex och påverkas starkt av mycket små variationer i vattnets sammansättning. Det är därför svårt att fastställa allmänt tillämpliga regler. Informaton i Figur 3 bygger på praktisk erfarenhet och ger riktlinjer för vissa olika typer av vatten.
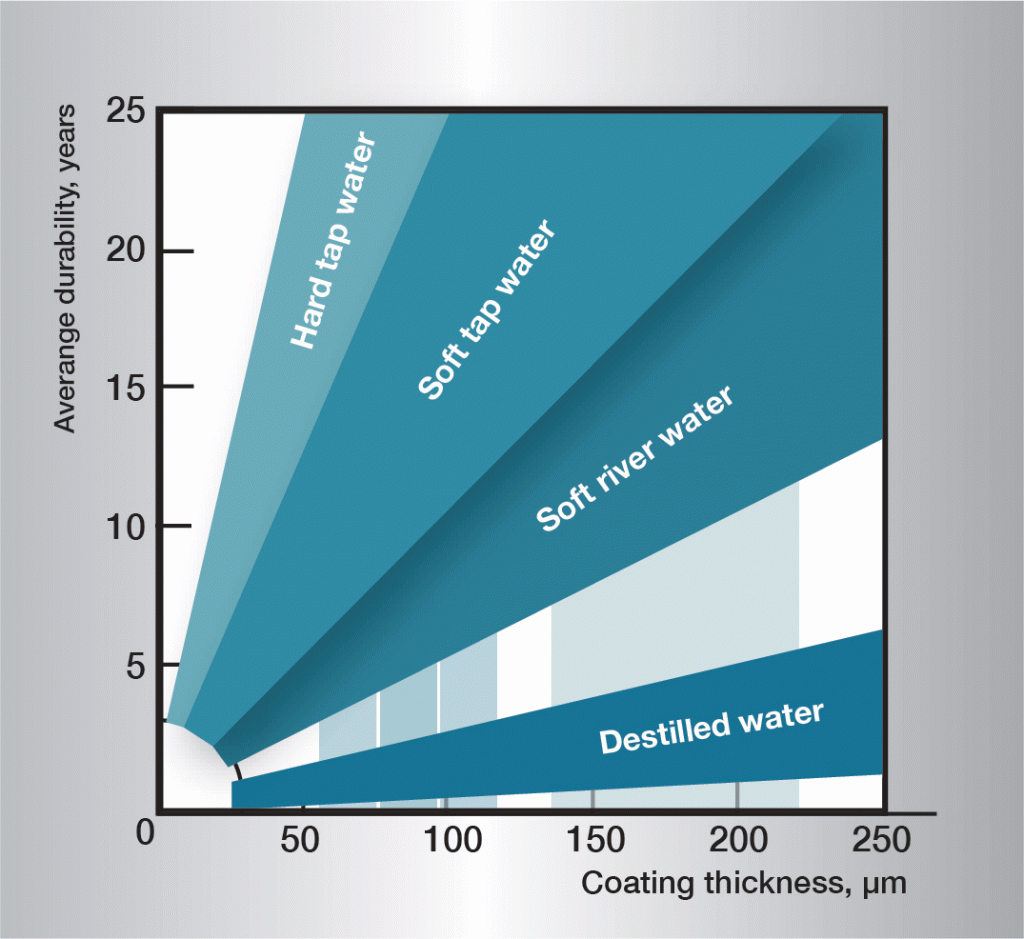
Fig. 3. Livslängd i olika vatten.,
Wet-storage stain
ibland visas ett vitt, floury och voluminöst lager som kallas wet-storage stain, eller vit rost, på galvaniserade ytor (fig.4). Vit rost bildas på material med nyförzinkade, blanka ytor och speciellt i sprickor mellan tätt packade ark, vinkeljärn och liknande material. En förutsättning är att materialet utsätts för kondens eller regnvatten under förhållanden där fukten inte kan avdunsta snabbt., Zinkytor som redan har fått ett normalt skyddande lager av korrosionsprodukter attackeras sällan. När zinkbeläggningar utsätts för luft bildas zinkoxid och zinkhydroxid. Under påverkan av koldioxid i luften omvandlas dessa till grundläggande zinkkarbonater. Om lufttillgången till zinkytan är begränsad, som i smala sprickor, får området otillräcklig koldioxid för att det normala skiktet av karbonater ska kunna bildas.
våtlagringsfläckskiktet är voluminöst och poröst och endast löst fastsatt på zinkytan., Som ett resultat existerar inte skydd mot fortsatt attack. Korrosion kan därför fortsätta så länge fukt kvarstår på ytorna. När våtlagringsfläcken har uppstått ska föremålet staplas så att ytorna kan torka snabbt. Detta kommer att stoppa attacken och, med fri tillgång till luft, kommer det normala skyddsskiktet att bildas. Den våta förvaringsfläcken tvättas gradvis bort och beläggningen förvärvar ett utseende som är normalt för exponerat, Varmförzinkat stål.,
eftersom denna vita korrosionsprodukt är mycket skrymmande (cirka 500 gånger den av zink från vilken den bildades) kan det tyckas vara allvarligt. Emellertid har våtlagringsfläcken ofta liten eller ingen betydelse för korrosionsskyddets livslängd. När det gäller mycket tunna beläggningar, t. ex. på elektropläterade föremål, kan en allvarlig attack av våtlagringsfläck vara av betydelse.
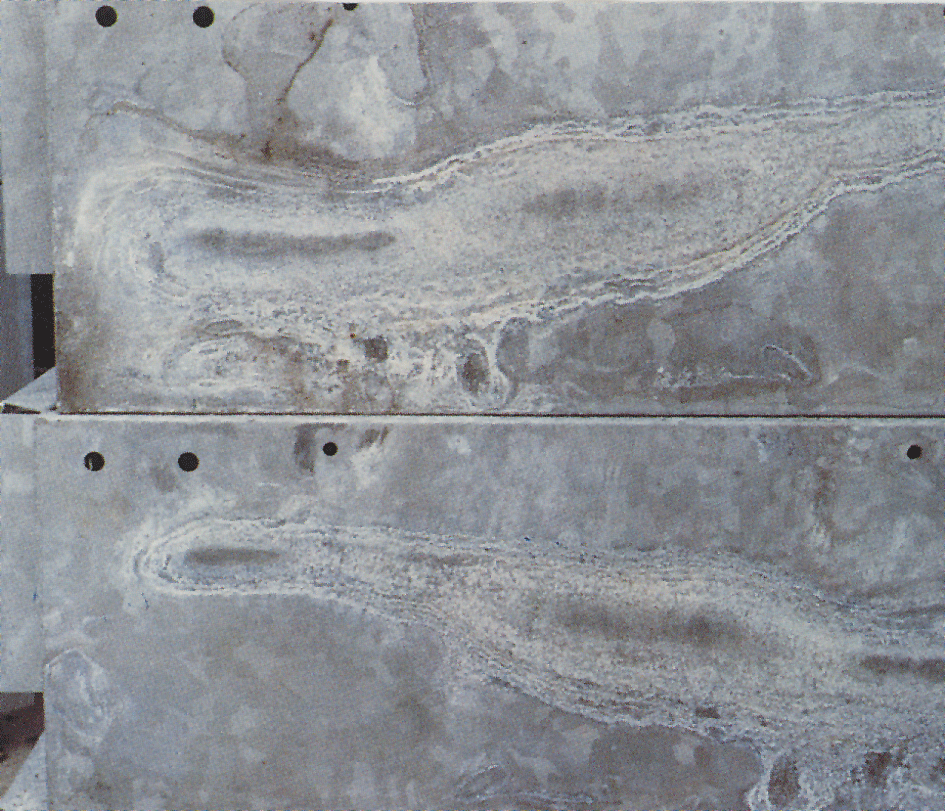
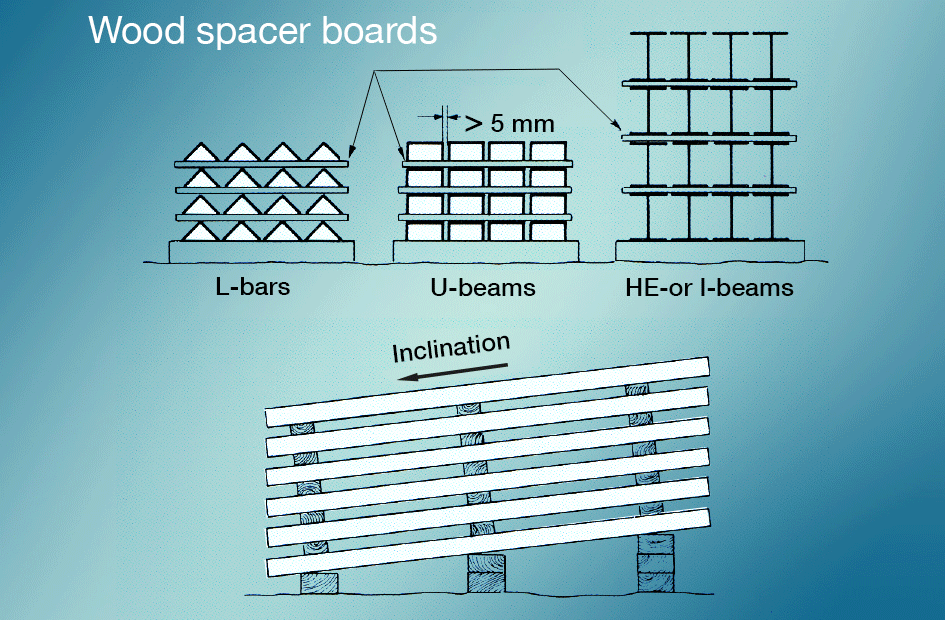
Våtförvaringsfläck undviks bäst genom att förhindra att nyförzinkade ytor kommer i kontakt med regn eller kondensat under transport., Material som förvaras utomhus bör staplas så att vatten kan rinna av lätt och så att alla ytor är väl ventilerade (fig. 5). Målning efter galvanisering ger mycket bra skydd.
korrosion i jord
korrosionsförhållandena i jord är mycket komplicerade och variationer kan vara stora mellan olika platser, även de i närheten av varandra. Jord kan innehålla vittrade produkter, fria eller bundna salter, syror och alkalier, blandningar av organiska ämnen, oxiderande eller reducerande svampar, mikroorganismer etc., Beroende på dess struktur har jorden olika grader av permeabilitet för luft och fukt. Normalt är syrehalten mindre än i luft, medan koldioxidinnehållet är högre.
svenska jordar är i allmänhet inte särskilt aggressiva. Genomsnittlig korrosion för zink tas vanligtvis som 5 µm per år. Allvarligt aggressiva jordar ses sällan. I Nord-och Västbotten kan marken innehålla svavel. De är ofta svarta, men lätta när de utsätts för luft. I dessa jordar är zinkkorrosionshastigheter mycket höga.
en metod för att bestämma en Marks korrosivitet är att mäta dess resistivitet., Om jordens resitivitet inte kan fastställas kan de tumregler som anges i Figur 6 ge en vägledning. När det gäller exponering av metaller mot jord är det dock lämpligt att söka expertråd från lämpligt kvalificerade källor.

galvanisk korrosion

om två olika metaller eller legeringar, helt eller delvis omgivna av en elektrolyt, är anslutna skapas en galvanisk cell. Vilken metall blir anoden eller katoden bestäms av deras elektrodpotentialer i den aktuella elektrolyten. I havsvatten, vilket motsvarar de flesta praktiska förhållanden, tar vissa metaller och legeringar upp olika positioner på elektrokemisk skala, som visas i Figur 7.,
om stål är anslutet till koppar eller mässing blir stålet anoden i cellen och korroderar. Om stål är anslutet till kadmium, aluminium, zink eller magnesium blir det katoden och skyddas mot korrosion, medan anodmetallen konsumeras. Galvanisk korrosion kallas också bimetallisk korrosion och används för att skydda undervattensstrukturer mot korrosion, när det kallas katodiskt skydd.
katodiskt skydd som ges av zinkbeläggningar
i varmförzinkat stål är zink och stål i god elektrisk kontakt med varandra., Om zinkbeläggningen är skadad i närvaro av en elektrolyt skapas en galvanisk cell. Elektrolyten kan vara kondensat eller regnvatten. Ibland kan hela strukturen nedsänkas i vätska. I denna cell blir zinken anoden eller upplösningspolen, det exponerade stålet blir katoden och skyddas därför mot korrosion.
i inledningsfasen är det ofta möjligt att se en svag ust-bildning på den exponerade delen av stålytan där beläggningen har skadats, men efter ett tag bildar vitaktiga grå områden som gradvis sprider sig över hela det skadade området., Zinkbeläggningen korroderar och sparsamt lösliga zinklegeringar faller ner till katodytan där de skyddar stålet från fortsatt rostangrepp. Detta kallas ofta ”självläkande”, vilket är något av en missvisande eftersom zinkskiktet naturligtvis inte återställs.
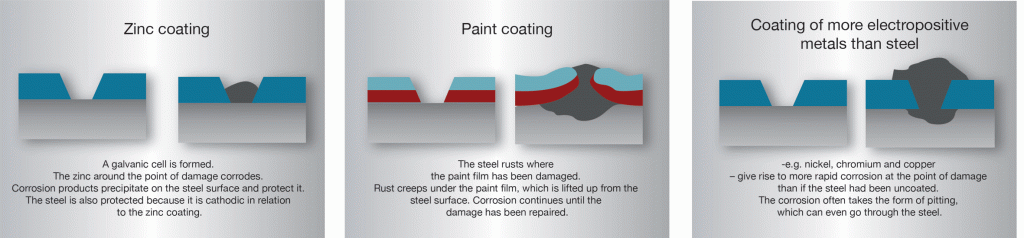
på grund av zinkens katodskydd kan rost inte ”krypa in” under beläggningen vid skadans punkt på det sätt som det kan krypa under filmer av färg eller beläggningar av metaller mer ädla än stål., Zinkbeläggningar på stål är ovanliga, eftersom ett ganska stort område av skador på beläggningen inte orsakar katastrofal förlust av rostskydd. Utbudet av katodiskt skydd är beroende av elektrolytens natur som skapar cellen. För strukturer i normala atmosfärer är det vanligt att förvänta sig skyddande verkan över flera millimeter. I havsvatten kan dock betydligt större avstånd förväntas.
zinkbeläggningar i kontakt med icke-järnmetaller
den elektrokemiska potentialskalan visar att zink är mindre ädelt än de flesta vanliga metaller. Detta innebär att när zink är ansluten till dessa metaller i en galvanisk cell är det zink som blir den upplösande Polen. I princip bör sådana anslutningar därför undvikas när det är möjligt. En bra metod är att använda en isolator som plast eller gummi vid fogen.,
Aluminium och rostfritt stål kan ofta anslutas direkt till galvaniserat material i luft eller ganska torra miljöer utan märkbar korrosion. Men i vatten bör en isolator alltid användas.
Koppar och kopparlegeringar är mer elektriskt aktiva och det finns ofta en frisättning av kopparjoner som sprids över stora ytor och orsakar märkbar attack. Av denna anledning bör dessa metaller aldrig tillåtas komma i kontakt med galvaniserat stål och en isolator ska användas.,
Varmförzinkat stål i kontakt med murbruk, gips och trä
fuktig murbruk och gips attack zink. Attacken upphör när materialet torkar ut. Torrt eller måttligt fuktigt trä, både impregnerat och oinmpregnerat, kan spikas med varmförzinkade naglar till god effekt. Men när det gäller naglar eller gängade fackföreningar som ständigt utsätts för vatten föredras ett syrabeständigt material. Andra torra byggmaterial, såsom mineralull, attackerar inte zink.,
förpackning och transport av galvaniserat stål
Även om en varmförzinkad beläggning kan motstå ganska grov behandling bör den hanteras med försiktighet under lagring och transport. Vid långa varor enkel packning och bindning till buntar inte bara skyddar mot mekaniska skador, men det underlättar ofta transporten själv. Förpackning och bindning bör dock ske på ett sådant sätt att risken för våt lagringsstam undviks. Distanser bör användas för att förhindra sådana attacker.