Glykosidbindningsbildning
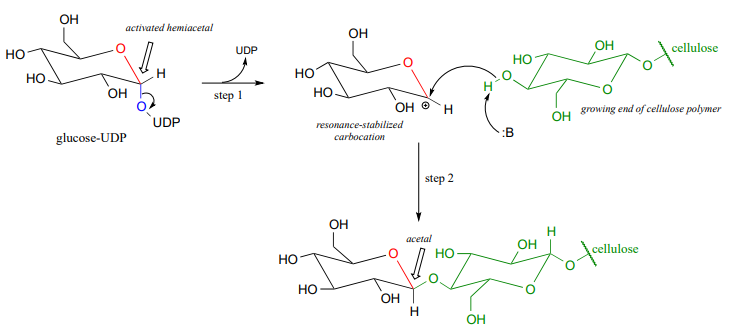
låt oss nu överväga acetalbildning i ett biokemiskt sammanhang. Ett mycket viktigt exempel på acetal / ketalgruppen i biokemi är de glykosidbindningar som kopplar enskilda sockermonomerer till att bilda polysackarider (se Avsnitt 1.3 för en snabb genomgång)., Titta på den glykosidbindningen mellan två glukosmonomerer i en cellulaskedja:
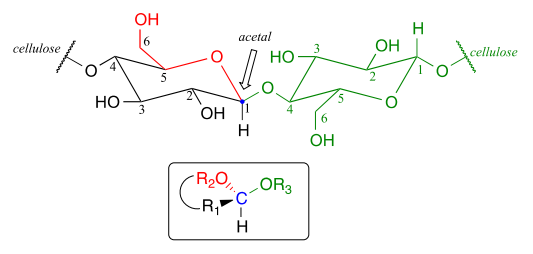
om du tittar noga bör du känna igen att Kol #1, Det anomeriska kolet på den vänstra glukosmonomeren, är det centrala kolet i en acetalgrupp. Biokemister hänvisar till detta som en b-1,4-koppling, eftersom stereokemi vid kol #1 är B i det specialiserade kolhydratnomenklatursystemet, och det är kopplat till kol #4 av nästa glukos på kedjan., Den stora strukturella mångfalden av kolhydrater härrör till stor del från de olika kopplingarna som är möjliga – både när det gäller vilka två kol är kopplade, och även stereokemi av kopplingen. Du kommer att se många fler variationer av glykosidbindningslänkmönster om du studerar kolhydratbiokemi i större djup.,
reaktioner där nya glykosidbindningar bildas katalyseras av enzymer som kallas glykosyltransferaser, och i organiska kemitermer representerar dessa reaktioner omvandlingen av en hemiacetal till en acetal (kom ihåg att sockermonomerer i sin cykliska form är hemiacetaler och hemiketaler)., Mekanismen för glykosidbindningsbildning i en levande cell paralleller den syrakatalyserade (icke-biologiska) acetalbildande mekanismen, med en viktig skillnad: i stället för att protoneras omvandlas \(OH\) – gruppen av hemiacetalen till en bra lämnande grupp genom fosforylering (detta är ett mönster som vi är bekanta med från kapitlen 9 och 10). Den specifika identiteten hos den aktiverande fosfatgruppen varierar för olika reaktioner, så den generaliseras i figuren nedan.,
mekanism för (biokemisk) acetalbildning:
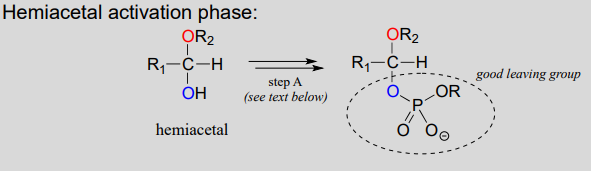
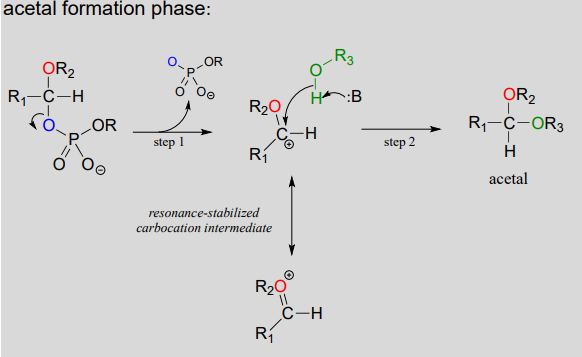
- steg a (Aktiveringsfas): denna reaktionsfas varierar beroende på det enskilda fallet, men alltid beroende på vilken typ av reaktion som används.omfattar fosfatgruppsöverföringssteg som är bekanta från kapitel 9. Vad som är viktigast för vår nuvarande diskussion är dock helt enkelt att hydroxylgruppen på hemiacetal har aktiverats-dvs. tillverkad i en bra lämnar grupp-genom fosforylering.,
- Steg 1: Nu när den avgående gruppen har aktiverats gör den sitt jobb och lämnar, vilket resulterar i en resonansstabiliserad karbocation.
- steg 2: en nukleofil alkohol på den växande cellulosakedjan angriper den högelektrofila karbocationen för att bilda en acetal. Här bestäms stereokemi hos den nya glykosidbindningen: beroende på reaktionen kan alkoholnukleofilen närma sig från vardera sidan av den plana karbokaden.,
för att upprepa: det är viktigt att känna igen det välbekanta \(S_N1\) mekanistiska mönstret i spel här: i steg A omvandlas en dålig lämnar grupp till en bra lämnar grupp, i steg 1 lämnar den lämnar gruppen och en stabiliserad carbocation är kvar, och i steg 2 en nukleofil attacker för att bilda en ny bindning och slutföra substitutionsprocessen. Titta tillbaka på de\ (S_N1\) reaktioner vi såg i kapitel 8 Om du har problem med att göra denna mekanistiska anslutning.,
nu, låt oss titta specifikt på glykosyltransferasreaktionsmekanismen där en ny glykosidbindning bildas på en växande cellulosakedja. Glukos (en hemiacetal) aktiveras först genom två enzymatiska fosfatöverföringssteg: steg A1, en fosfatisomeriseringsreaktion med en mekanism som liknar reaktionen i problem P9. 13, följt av ett UTP-beroende steg A2, för vilket du uppmanades att föreslå en mekanism i problem P9.12.,
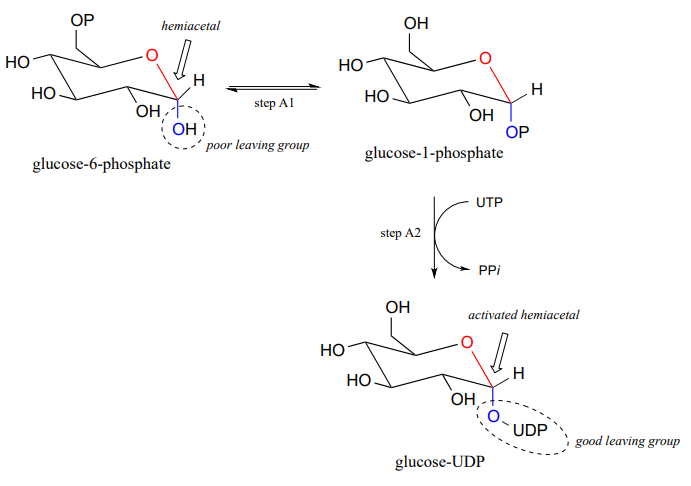
UDP-gruppen på glukos-UDP lämnar sedan (steg 1 nedan) och bildar en resonansstabiliserad förkolning mellanliggande. Attack av alkoholgruppen på den växande cellulosakedjan i steg 2 bildar den glykosidiska (acetal) bindningen. Notera inversion av stereokemi.