catálise heterogénea
em catálise heterogénea, o catalisador está numa fase diferente dos reagentes. Pelo menos um dos reagentes interage com a superfície sólida em um processo físico chamado adsorção de tal forma que uma ligação química no reagente se torna fraca e então quebra. Venenos são substâncias que se ligam irreversivelmente aos catalisadores, impedindo reagentes de adsorver e, assim, reduzindo ou destruindo a eficiência do catalisador.,um exemplo de catálise heterogênea é a interação do hidrogênio gasoso com a superfície de um metal, como Ni, Pd ou Pt. Como mostrado na parte A) da figura \(\PageIndex{2}\), as ligações hidrogénio–hidrogénio quebram e produzem átomos de hidrogénio adsorvidos individualmente na superfície do metal. Como os átomos adsorvidos podem se mover na superfície, dois átomos de hidrogênio podem colidir e formar uma molécula de hidrogênio gasoso que pode então deixar a superfície no processo inverso, chamado dessorção. Átomos adsorvidos em uma superfície de metal são substancialmente mais reativos do que uma molécula de hidrogênio., Como a ligação H–H relativamente forte (energia de dissociação = 432 kJ/mol) já foi quebrada, a barreira de energia para a maioria das reações de H2 é substancialmente menor na superfície do catalisador.
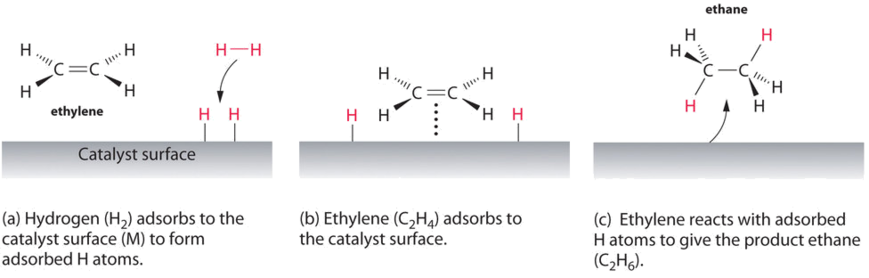
Figura \(\PageIndex{2}\) mostra um processo chamado de hidrogenação, na qual os átomos de hidrogênio são adicionados para a ligação dupla de um alkene, tais como eteno, para dar um produto que contém C–C simples obrigações, no caso do etano., A hidrogenação é usada na indústria alimentar para converter óleos vegetais, que consistem em longas cadeias de alcenos, em derivados sólidos mais valiosos comercialmente que contêm cadeias de alquilo. A hidrogenação de algumas das ligações duplas em óleos vegetais polinsaturados, por exemplo, produz margarina, um produto com um ponto de fusão, textura e outras propriedades físicas semelhantes às da manteiga.
vários exemplos importantes de reacções catalíticas heterogéneas industriais estão na tabela \(\PageIndex{1}\)., Embora os mecanismos destas reacções sejam consideravelmente mais complexos do que a simples reacção de hidrogenação descrita aqui, todas elas envolvem adsorção dos reagentes numa superfície catalítica sólida, reacção química das espécies adsorvidas (por vezes através de uma série de espécies intermédias) e, finalmente, dessorção dos produtos da superfície.