heterogene katalyse
bij heterogene katalyse bevindt de katalysator zich in een andere fase dan de reagentia. Ten minste één van de reagentia interageert met het vaste oppervlak in een fysisch proces dat adsorptie wordt genoemd op een zodanige wijze dat een chemische binding in de reactieve stof zwak wordt en dan breekt. Vergiften zijn stoffen die zich onherroepelijk aan katalysatoren binden, waardoor reagentia niet worden geadsorbeerd en de efficiëntie van de katalysator wordt verminderd of vernietigd.,
een voorbeeld van heterogene katalyse is de interactie van waterstofgas met het oppervlak van een metaal, zoals Ni, Pd of Pt. Zoals getoond in Deel (A) in Figuur \(\Pagindex{2}\), breken de waterstof–waterstofbindingen en produceren ze individueel geadsorbeerde waterstofatomen op het oppervlak van het metaal. Omdat de geadsorbeerde atomen op het oppervlak kunnen bewegen, kunnen twee waterstofatomen botsen en een molecuul waterstofgas vormen dat vervolgens het oppervlak in het omgekeerde proces kan verlaten, genaamd desorptie. Geadsorbeerde H-atomen op een metaaloppervlak zijn aanzienlijk meer reactief dan een waterstofmolecuul., Omdat de relatief sterke H-H binding (dissociatie-energie = 432 kJ / mol) al is verbroken, is de energiebarrière voor de meeste reacties van H2 aanzienlijk lager op het katalysatoroppervlak.
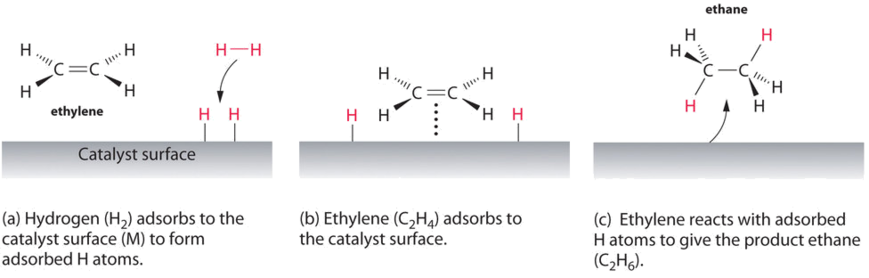
figuur \(\Paginindex{2}\) toont een proces dat hydrogenering wordt genoemd, waarbij waterstofatomen worden toegevoegd aan de dubbele binding van een alkeen, zoals ethyleen, om een product te verkrijgen dat C–C enkelvoudige bindingen bevat, in dit geval ethaan., Hydrogenering wordt gebruikt in de voedingsindustrie om plantaardige oliën, die bestaan uit lange ketens van alkenen, om te zetten in meer commercieel waardevolle vaste derivaten die alkylketens bevatten. Hydrogenering van sommige van de dubbele bindingen in meervoudig onverzadigde plantaardige oliën, bijvoorbeeld, produceert margarine, een product met een smeltpunt, textuur en andere fysische eigenschappen die vergelijkbaar zijn met die van boter.
verschillende belangrijke voorbeelden van industriële heterogene katalytische reacties staan in Tabel \(\Paginindex{1}\)., Hoewel de mechanismen van deze reacties aanzienlijk complexer zijn dan de hier beschreven eenvoudige hydrogeneringsreactie, omvatten zij alle adsorptie van de reagentia aan een vast katalytisch oppervlak, chemische reactie van de geadsorbeerde soorten (soms via een aantal tussenliggende soorten) en tenslotte desorptie van de producten van het oppervlak.