En kort oppsummering av Haber Prosessen
Haber Prosessen kombinerer nitrogen fra luften med hydrogen stammer hovedsakelig fra naturgass (metan) i ammoniakk. Reaksjonen er reversibel og produksjon av ammoniakk er eksoterme.,
![]()
![]()
En flyt ordningen for Haber Prosessen ser ut som dette:
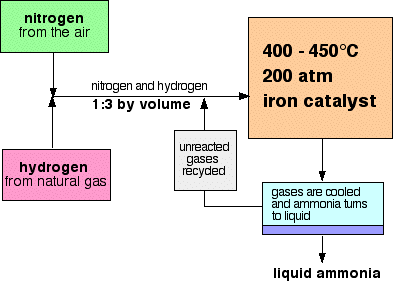
Noen merknader om forhold som
katalysator
The catalyst er faktisk litt mer komplisert enn rent jern. Det har kaliumhydroksid lagt til det som en pådriver – et stoff som øker sin effektivitet.
trykk
trykket varierer fra en fabrikk til en annen, men er alltid høy. Du kan ikke gå langt galt i en eksamen sitere 200 atmosfærer.,
Resirkulering
På hver pass av gasser gjennom reaktoren, bare ca 15% av nitrogen og hydrogen konverterer til ammoniakk. (Dette tallet også varierer fra plante til plante.) Ved kontinuerlig gjenvinning av ureagert nitrogen og hydrogen, den generelle konvertering er ca 98%.
å Forklare forhold som
Den andelen av nitrogen og hydrogen
blanding av nitrogen og hydrogen går inn i reaktoren er i forholdet 1 volum av nitrogen til 3 volumer av hydrogen.,
Avogadro ‘ s Lov sier at like volumer av gasser ved samme temperatur og trykk inneholde like mange molekyler. Det betyr at gasser går inn i reaktoren i forholdet 1 molekyl av nitrogen til 3 av hydrogen.
Det er andelen som kreves av ligningen.
I noen reaksjoner som du kan velge å bruke et overskudd av en av reaktantene. Du vil gjøre dette hvis det er spesielt viktig å bruke opp så mye som mulig av andre reaktant – hvis, for eksempel, det var mye dyrere. Det gjelder ikke i dette tilfellet.,
Det er alltid en ned-side til å bruke noe annet enn ligningen proporsjoner. Hvis du har et overskudd av en reaktant det vil være molekyler som passerer gjennom reaktoren som ikke kan muligens reagere fordi det ikke er noe for dem til å reagere med. Dette er sløsing med reaktoren plass – særlig plass på overflaten av katalysator.
temperaturen
Likevekt hensyn
Du trenger å skifte posisjon i likevekt så langt som mulig til høyre for å produsere den høyeste, mulige beløpet av ammoniakk i likevekt blandingen.,
Den frem reaksjon (produksjon av ammoniakk) er eksoterme.
![]()
![]()
Ifølge å Le Chatelier ‘ s Prinsipp, vil dette være å foretrekke hvis du senke temperaturen. Systemet vil reagere ved å flytte plasseringen av likevekt for å motvirke dette – med andre ord ved å produsere mer varme.
for å få så mye ammoniakk som mulig i likevekt blanding, må du så lav temperatur som mulig. Imidlertid, 400 – 450°C er ikke en lav temperatur!,
Pris hensyn
Jo lavere temperatur du bruker, jo tregere reaksjon blir. En produsenten prøver å produsere så mye ammoniakk som mulig per dag. Det gir ingen mening å prøve å oppnå en likevekt blanding som inneholder en svært høy andel av ammoniakk hvis det tar flere år for reaksjon for å oppnå likevekt.
Du trenger gasser for å nå likevekt innen svært kort tid at de vil være i kontakt med katalysator i reaktoren.,
kompromiss
400 – 450°C er et kompromiss temperatur produsere en rimelig høy andel av ammoniakk i likevekt blanding (selv om det er bare 15%), men i en svært kort tid.
trykk
Likevekt hensyn
![]()
![]()
legg Merke til at det er 4 molekyler på venstre side av ligningen, men bare 2 på høyre side.,
Ifølge å Le Chatelier ‘ s Prinsipp, hvis du øker trykket i systemet vil reagere ved å favorisere den reaksjonen som gir færre molekyler. Det vil føre til press for å falle igjen.
for å få så mye ammoniakk som mulig i likevekt blanding, må du så høyt trykk som mulig. 200 atmosfærer er et høyt press, men ikke utrolig høyt.
Pris hensyn
å Øke trykket bringer molekyler tettere sammen., I dette spesielle tilfellet, vil det øke sjansen for treff og fester seg til overflaten av katalysator hvor de kan reagere. Jo høyere trykket, jo bedre i form av prisen av en gass reaksjon.
Økonomiske hensyn
Veldig høyt press er svært dyre å produsere på to tellinger.
Du har til å bygge ekstremt sterk rør og oppbevaring fartøy for å tåle svært høye trykk. Det øker din kapital når anlegget er bygget.
Høyt press koster mye å produsere og vedlikeholde., Det betyr at de løpende kostnadene for anlegget ditt er svært høy.
kompromiss
200 atmosfærer er et kompromiss press valgt på økonomisk grunnlag. Hvis trykket som brukes er for høy, kostnaden av å produsere det overstiger den pris du kan få for ekstra ammoniakk produseres.
katalysator
Likevekt hensyn
The catalyst har ingen effekt på plasseringen av likevekt. Legge til en katalysator ikke gir noen større prosentandel av ammoniakk i likevekt blandingen. Dens eneste funksjon er å øke hastigheten på reaksjonen.,
Pris hensyn
I fravær av en katalysator reaksjonen er så treg at nesten ingen reaksjon skjer i enhver fornuftig tid. Den katalysatoren som sikrer at reaksjonen er rask nok for en dynamisk likevekt til å bli satt opp i løpet av svært kort tid at gassene er faktisk i reaktoren.
Skille ammoniakk
Når gasser forlater reaktoren de er varme, og på et veldig høyt trykk., Ammoniakk er lett flytende under trykk, så lenge det ikke er for varmt, og så temperaturen i blandingen er senket nok for ammoniakk til å slå til en væske. Nitrogen og hydrogen forbli som gasser selv under disse høye trykk, og kan resirkuleres.
Spørsmål for å teste din forståelse
Hvis dette er det første settet av spørsmål du har gjort, kan du lese innledende side før du starter. Du må bruke TILBAKE-KNAPPEN i nettleseren din for å komme tilbake hit etterpå.,
spørsmål på Haber Prosessen
svar
Hvor ønsker du å gå nå?
Til likevekt-menyen . . .
Til Fysisk Kjemi-menyen . . .
Til Hovedmenyen . . .