닐 대체의 수산기 그룹
화학적 행위의 할로겐화물 알킬 사용할 수 있습에 참조로 발견 유사 대체 및 제거반응의 알코올. 주요한 차이점은 물론 할라이드에서 수산화물로 떠나는 음이온의 변화입니다. 산소는 염소보다 약간 더 전기 음성이기 때문에(폴링 스케일에서 3.5 대 2.8),C-O 결합은 C-Cl 결합보다 더 극성 일 것으로 예상된다., 또한,독립적이 측정의 electrophilic 적 특성의 탄소원자에서 자신의 NMR 화학적 변화(두 13C 및 알파 양성자)나타내는 산소 및 염소 치환을 발휘와 유사한 전자 인출 영향력을 때에 결합 sp3 혼 탄소 원자를 함유하고 있습니다. 에도 불구하고 이 유망한 배경의 증거,알콜지 않을 겪는 동 SN2 반응을 일반적으로 관찰 할로겐화물 알킬. 예를 들어 급속한 SN2 반응의 1-bromobutane 나트륨 시안화물,아래와 같은 병렬할 때 1-부탄올 치료 나트륨 시안화., 사실,에틸 알코올은 종종 이와 같은 알킬 할라이드 치환 반응을위한 용매로 사용됩니다.
CH3CH2CH2CH2–Br+Na(+)CN(–) CH3CH2CH2CH2–CN+Na(+)Br(–)
CH3CH2CH2CH2–CN+Na(+)Br(–)
CH3CH2CH2CH2–OH Na(+)CN(–)  아무 반응
아무 반응
핵심 요소기의 안정성을 떠나는 음이온(브롬 대 수산화물)., HBr 은 물보다 훨씬 강한 산이며(크기가 18 개 이상),이 차이는 각각의 공액 염기를 생성하는 반응에 반영됩니다. 약한 기초,브로마이드,더 안정적이고리에서 교체 또는 철폐의 반응은 훨씬 더 유리한다는 것의 수산화물이온,보다 강력하고 더 적은 안정적인 기초입니다.
명확한 단계 개선의 반응성에서 알콜 SN2 반응하는 것을 수정하–오 기능 그룹에서는 방법을 향상시키는 그것의 안정성으로 떠나는 음이온., 그러한 변형 중 하나는 강산에서 치환 반응을 수행하여–OH 를–OH2(+)로 전환시키는 것이다. 기 때문에 hydronium 이온(H3O(+))이 훨씬 더 강한 산상 물,의 어원이 기본(H2O)은 더 나은 그룹을 떠나보다 수산화물이온. 유일한 문제와 이 전략은 많은 nucleophiles 포함하여,시안화물,비활성화하여 지금 바로 이에 강산,효과적으로 제거하 닐 co-반응에 필요한 변경하십시오., 강산 HCl,HBr 및 HI 는 공액 염기가 양호한 친핵체이며 알코올보다 약한 염기이기 때문에 이러한 어려움의 대상이 아닙니다. 다음 방정식은 이러한 산에 의해 영향을받을 수있는 알코올의 일부 치환 반응을 설명합니다. 알킬 할라이드와 마찬가지로,1º-알콜의 친 핵성 치환은 SN2 메커니즘에 의해 진행되는 반면,3º-알콜은 SN1 메커니즘에 의해 반응한다. 2º 알콜의 반응은 두 메커니즘 모두에 의해 발생할 수 있으며 종종 일부 재 배열 된 생성물을 생성합니다., 괄호 안의 숫자는 다음을 광산의 수식을 나타내는 무게의 비율이 집중된 수용액 양식에서는 이산은 일반적으로 사용됩니다.
이러한 반응을 때때로”산 촉매 화”라고하지만,이는 엄격하게 정확하지 않습니다. 에서 전반적으로 변신,강한 HX 산으로 변환하는 물,약산,그래서 적어도 stoichiometric 의 양 HX 에 필요한 완벽한 변환에 알코올의 할로겐화 알킬., 를 사용의 필요성에 해당의 양이 매우 강한 산에서 이러한 반응한 그 유용성을 간단한 알코올의 유형은 다음과 같다. 산에 민감한 그룹을 가진 알코올은 물론 그러한 치료를 용납하지 않습니다. 그럼에도 불구하고,의 아이디어를 수정하-오 기능 그룹을 그것의 안정성을 향상으로 떠나는 음이온이 추구될 수 있는 다른 방향으로. 다음 다이어그램은 효과가 입증 된 몇 가지 수정 사항을 보여줍니다. 각각의 경우에 수산기는 강산의 에스테르로 전환된다. 처음 두 예는 앞에서 설명한 술포네이트 에스테르를 나타낸다., 세 번째와 네 번째 예는 표시의 형성 아인산염 에스테르(X 을 나타냅의 나머지 bromines 또는 추가 알코올 치환기)및 chlorosulfite 에스테르,각각합니다. 이러한 모든 떠나 집단(파란색)의 어원이산하는 것보다 훨씬 더 강한 물(13-16 권의 십);따라서,떠나는 음이온이 이에 대응하여 더 안정적 수산화물이온. 상기 메실 레이트 및 토실 레이트 화합물은 다양한 친핵체와의 치환 반응에 사용될 수 있기 때문에 특히 유용하다., 중간체에서 생산되는 반응의 알코올로 인 tribromide 과 티오닐 클로라이드 염화나(마지막 두 가지 예)는 드물게 고립 된,그리고 이러한 반응을 생산하기 위해 계속 알킬브로마이드 염화 제품입니다.
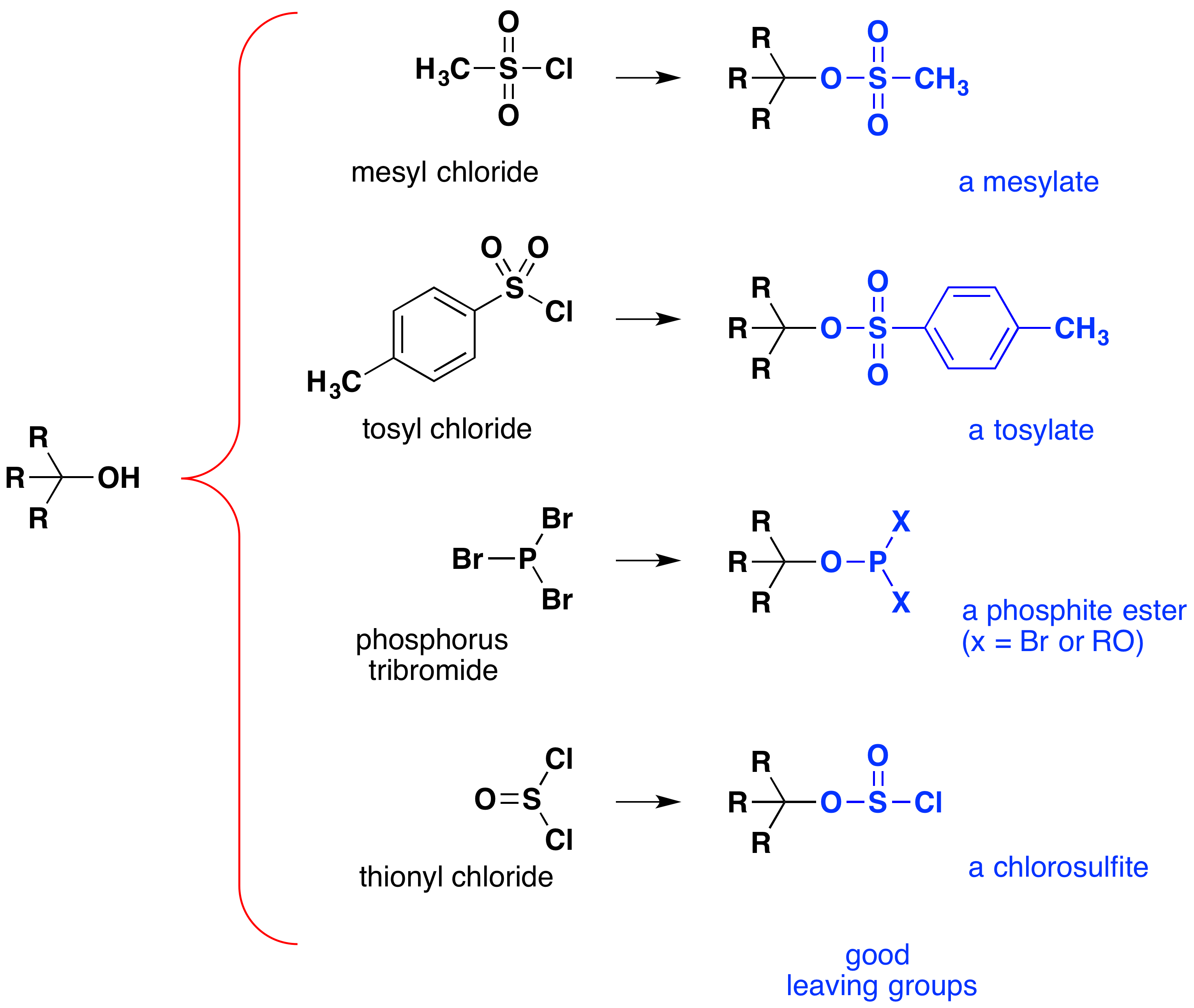
의 중요성 된 에스테르는 중간에서는 일반적인 닐 대체 반응의 알코올으로 설명될 수 있 다음의 전환 1-부탄올을 pentanenitrile(부틸리 시아나이드),반응 일어나지 않는 것으로 알코올 혼자입니다., 반면에 인 및 티 오닐 할라이드는 알콜을 상응하는 알킬 할라이드로 전환시키는 작용 만한다.,
| CH3CH2CH2CH2–OH + CH3SO2Cl | pyridine |
CH3CH2CH2CH2–OSO2CH3 | Na(+) CN(–) |
CH3CH2CH2CH2–CN + CH3SO2O(–) Na(+) |
Some examples of alcohol substitution reactions using this approach to activating the hydroxyl group are shown in the following diagram., 처음 두 경우에는 역할을 강화한다는 사실 설포의 유도체 에스테르 알코올을 수 있습 교체 할로겐화물 알킬에서의 다양한 SN2 반응입니다. 다음 두 사례는 알콜을 브롬화물로 전환시키는 데 인 트리 브로마이드의 사용을 입증합니다. 이 시약은 인산산 생성물이 HBr 보다 약한 산이기 때문에 염기(예:피리딘)를 첨가하지 않고 사용할 수 있습니다. 인 트리 브로마이드는 2º 알콜이 종종 경쟁 SN1 반응으로 인한 재 배열 부산물을 산출하기 때문에 1º 알콜과 함께 사용하는 것이 가장 좋습니다., 참고 에테르에서 산소 반응을 4 에 의해 영향을 받지 않 이 시약,반면 대안을 합성하여 집중 HBr 고대의 에테르. 인 삼염화붕소(PCl3)알코올로 변환하여 염화물 알킬 유사한 방식으로,그러나 티오닐 클로라이드 염화물은 일반적으로 선호하는을 위한 이러한 변화 때문에 무기물 제품은 가스(SO2&HCl). 인 triiodide 지 않은 안정되어 있지만 생성될 수 있습니다 현장에서의 혼합물에서 빨간 인과 요오드 및 행동 변환합 알코올을 알킬 요오드화물., 마지막 예는 티오 닐 클로라이드와 키랄 2º-알코올의 반응을 보여줍니다. 의 존재 유기 베이스와 같은 피리딘은 중요한 제공하므로 상당한 농도의 염화물 이온에 필요한 최종 SN2 반응의 chlorosufite 중간입니다., 의 부재에서 기초,chlorosufites 가열시 분해하여 수익률은 예상되는 염화 알킬로 보존 의 구성
차 알코올은 일반적으로 사용되지 않습에 대한 대체 반응의 형식이기 때문에 여기에서 설명 SN1 및 E1 반응 경로는 지배적 및 제어하기가 어렵기 때문입니다.

의 중요성 된 에스테르로 중간에 많은 대체 반응은 허황된 것이 아닙니다., SN2 반응에서 치환 부위에서 발생하는 구성 역전에 대한 엄격한 증거는 그러한 반응을 이용하게한다. 그러한 증거의 예가 아래에 표시됩니다. 보다 일반적으로 사용되는 술 포닐 유도체에 대한 약어는 다음 표에 주어진다.
| 설포닌 그룹 | CH3SO2– | CH3C6H4SO2– | BrC6H4SO2– | CF3SO2– |
|---|---|---|---|---|
| 이름&래그를 확장합니다., | Mesyl 또는 Ms | Tosyl Ts | Brosyl 또는 Bs | Trifyl 또는 Tf |
반전 증명

에 대한 자세한 토론의 수산기 교체 반응 및 설명의 다른 선택적인 방법이 변화에 대한 여기를 클릭하십시오.
기여자
- 윌리엄 레스 쉬,명예 교수(미시간 주 U.,), Virtual Textbook of Organic Chemistry