L’acciaio è il materiale più comune in uso oggi. Tuttavia, l’acciaio ha un grande svantaggio: il suo alto tasso di corrosione. La protezione delle strutture e dei componenti in acciaio è quindi di grande importanza economica.
La migliore protezione contro la corrosione dell’acciaio si ottiene con lo zinco. I rivestimenti di zinco sull’acciaio proteggono dalla corrosione in due modi:
- Con un effetto barriera, cioè impediscono all’ossigeno e all’umidità di raggiungere la superficie dell’acciaio.,
- Dando protezione catodica a graffi,scheggiature, bordi ecc.
Lo zinco è un metallo con un potenziale galvanico relativamente basso e un’alta tendenza alla corrosione. Tuttavia, il tasso di corrosione è basso nella maggior parte degli ambienti, poiché la superficie del rivestimento viene rapidamente coperta con prodotti corrosivi, che successivamente proteggono da ulteriore corrosione.
Corrosione nell’atmosfera
Quando un oggetto zincato a caldo lascia il bagno di zinco, la superficie dell’oggetto viene immediatamente attaccata dall’ossigeno nell’aria., Lo strato di ossido risultante ha pochissima capacità di proteggere dalla corrosione. Tuttavia, l’acqua e l’anidride carbonica nell’aria cambiano rapidamente lo strato di ossido in carbonati di zinco. Questi danno uno strato sigillato con un’adesione molto buona. Poiché i carbonati hanno una solubilità molto bassa in acqua, danno un’eccellente protezione alla superficie del rivestimento di zinco. La superficie lucida originale con una lucentezza metallica scompare per essere sostituita dal colore grigio chiaro opaco (fig.1).

Fig 1., Superficie esposta di un rivestimento di zinco con strato esterno di zinco puro. La superficie lucida scompare per essere sostituita da prodotti di corrosione grigi (a volte chiamati patina di zinco).

Fig. 2. Superficie scolorita sulla colonna di illuminazione. Il rivestimento è costituito principalmente da una lega di ferro-zinco che si estende alla superficie. Il ferro è esposto durante la corrosione, che porta alla formazione di ruggine. È solo ruggine superficiale ed è solo di significato estetico.,
L’aria esterna contiene una quantità maggiore o minore di elementi corrosivi — gas, fuliggine, umidità (nebbia, rugiada, pioggia, neve), polvere inerte e aggressiva. I livelli possono variare con la posizione e il periodo dell’anno. I solfati e i solfiti di zinco sono solubili in acqua e hanno scarsa adesione alla superficie dello zinco. Sono quindi lavati via facilmente dalla pioggia. Una superficie di zinco fresca viene quindi esposta all’attacco dell’ossigeno nell’aria e il ciclo di corrosione viene ripetuto. La corrosione nell’aria contenente ossidi di zolfo è quindi maggiore che nell’aria pulita., Tuttavia, la quantità di anidride solforosa nell’atmosfera è diminuita drasticamente negli ultimi anni, e di conseguenza anche la corrosione dello zinco è diminuita.
In ambienti marini, la corrosione dello zinco è influenzata dal contenuto di sale dell’aria. Tuttavia, l’aria marina contiene piccole quantità di sali di magnesio, con buone influenze passivanti. La corrosione non è quindi così grande come ci si potrebbe aspettare. Il contenuto di sale dell’aria si riduce rapidamente lontano dalla costa.
La corrosione dello zinco è influenzata da molti fattori., Ciò significa che non è possibile fornire una formula generalmente applicabile per i tassi di corrosione. I rivestimenti dello zinco, tuttavia, sono stati utilizzati a lungo, in una vasta gamma di condizioni, per proteggere l’acciaio dalla ruggine. È stato condotto anche un gran numero di test a lungo termine. La conoscenza della corrosione dello zinco e dei tassi di corrosione in diversi ambienti è quindi buona. Oggi ci sono esempi di rivestimenti di zinco che sono stati esposti per più di cento anni.
Il colore dei prodotti corrosivi varia a seconda dell’ambiente in cui si formano., Gli ambienti marini danno prodotti di corrosione un po ‘ più bianchi rispetto agli ambienti rurali e urbani. I prodotti di corrosione sono solitamente più scuri negli ambienti urbani.
Corrosione nei liquidi
La superficie di zinco è generalmente coperta da uno strato protettivo di prodotti corrosivi quando è immersa in un liquido. Tuttavia, i liquidi possono essere acidi o alcalini e possono contenere particelle disciolte o solide di sostanze aggressive. Anche la temperatura e la portata del liquido sono importanti., Tutto ciò significa che lo strato protettivo può avere una composizione altamente variabile o non può formarsi affatto.
La corrosione elettrochimica, che svolge un ruolo subordinato nell’aria, è di maggiore importanza nei liquidi. L’entità della corrosione elettrochimica dipende dalla conduttività elettrica del liquido, che influenza l’influenza protettiva dello strato di zinco su aree più grandi o più piccole.
Il valore del pH del liquido è di maggior importanza. Il tasso di corrosione dello zinco è normalmente basso e stabile nell’intervallo di pH di 5,5-12,5, a temperature comprese tra 0 e 20 ° C., La corrosione al di fuori di questo intervallo è solitamente più rapida.
L’acqua dura, che contiene calce e magnesio, è meno aggressiva dell’acqua dolce. Insieme all’anidride carbonica queste sostanze formano carbonati scarsamente solubili sulla superficie dello zinco, proteggendo lo zinco da ulteriore corrosione.
L’acqua dolce spesso attacca lo zinco, poiché l’assenza di sali significa che lo strato protettivo non può essere formato.
Acque dolci aggressive possono essere trovate in molti fiumi e laghi in Finlandia, Norvegia, Svezia e ambienti simili.
Se la portata è maggiore di 0.,5 m / s la formazione dello strato protettivo sulla superficie dello zinco è inibita e la corrosione accelera.
La temperatura dell’acqua è di grande importanza per il tasso di corrosione. Al di sopra di circa 55 °C, i prodotti di corrosione che formano strati acquisiscono una struttura a grana grossa e perdono adesione alla superficie di zinco. Sono facilmente rimossi ed espongono zinco nuovo e fresco per un attacco di corrosione continuo e rapido. La velocità di corrosione raggiunge un massimo a circa 70 °C, dopo di che diminuisce in modo che a 100 °C sia all’incirca uguale a 50 °C.,
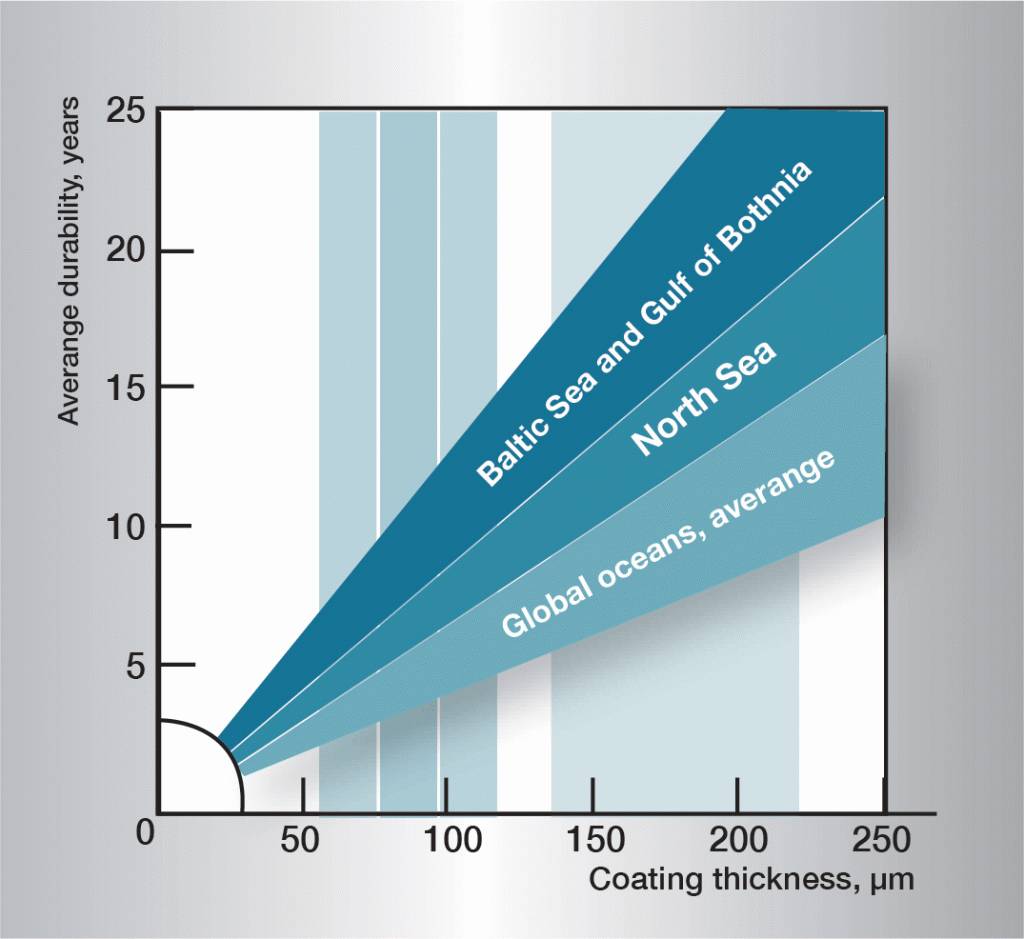
La sequenza di corrosione nell’acqua è molto complessa ed è fortemente influenzata da piccolissime variazioni nella composizione dell’acqua. È quindi difficile stabilire norme di applicazione generale. Le informazioni contenute nella figura 3 si basano sull’esperienza pratica e forniscono linee guida per alcuni diversi tipi di acqua.
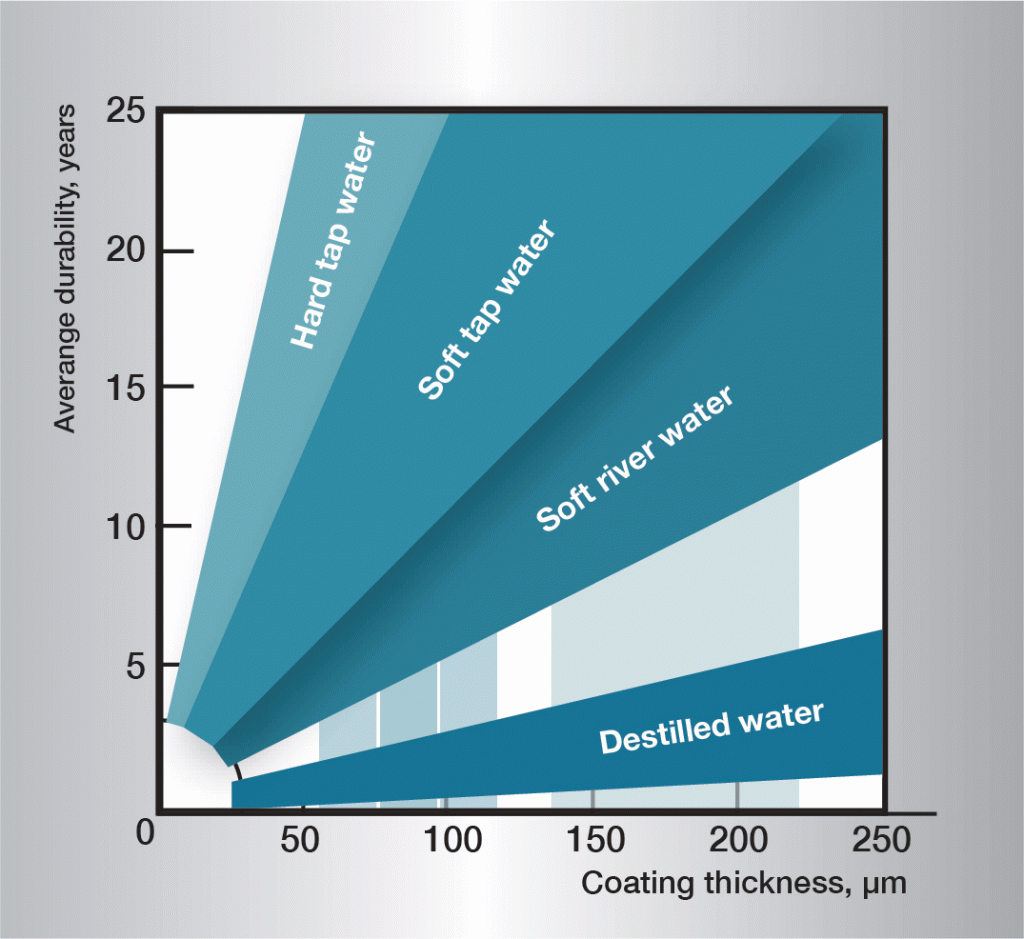
Fig. 3. Vita di servizio in diverse acque.,
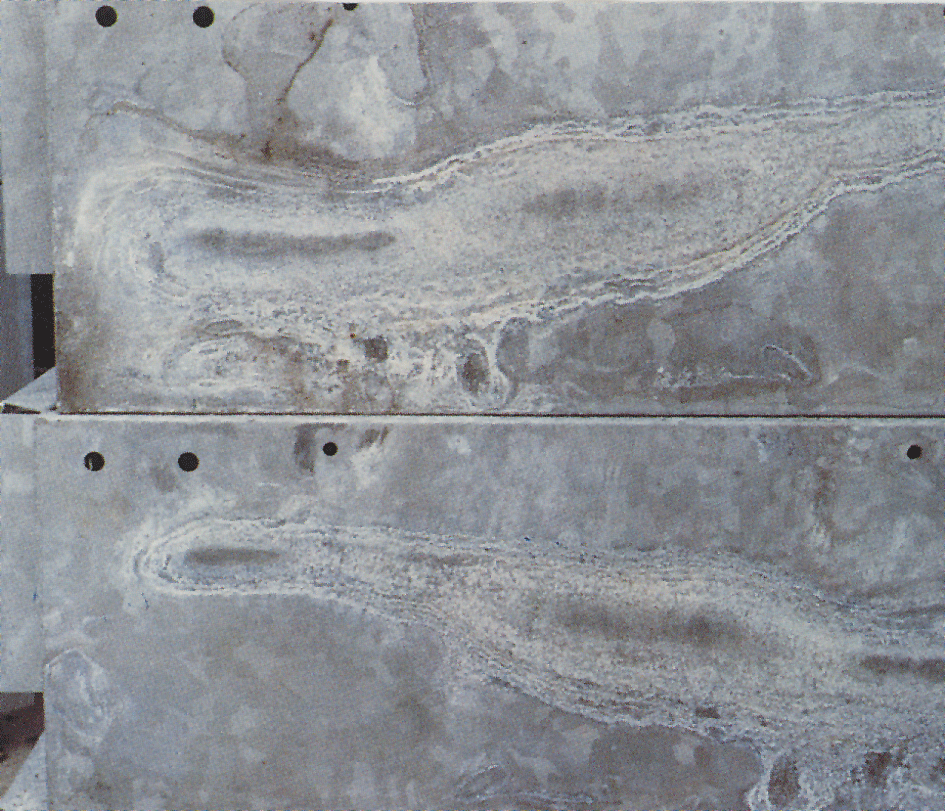
Wet-archiviazione macchia
a Volte bianca, farinosa e voluminoso strato chiamato wet-archiviazione macchia, o ruggine bianca, appare su superfici zincate (fig.4). La ruggine bianca si forma su materiali con superfici lucide e appena zincate e soprattutto in fessure tra fogli strettamente imballati, ferro angolare e materiali simili. Una condizione preliminare è che il materiale sia esposto a condensa o acqua piovana in condizioni in cui l’umidità non può evaporare rapidamente., Le superfici di zinco che hanno già ricevuto un normale strato protettivo di prodotti corrosivi vengono raramente attaccate. Quando i rivestimenti di zinco sono esposti all’aria, si formano ossido di zinco e idrossido di zinco. Sotto l’influenza dell’anidride carbonica nell’aria questi vengono convertiti in carbonati di zinco di base. Se l’accesso dell’aria alla superficie di zinco è limitato, come nelle fessure strette, l’area riceve anidride carbonica insufficiente per consentire la formazione del normale strato di carbonati.
Lo strato di macchia bagnato-stoccaggio è voluminoso e poroso e solo vagamente attaccato alla superficie di zinco., Di conseguenza, la protezione contro l’attacco continuo non esiste. La corrosione può quindi continuare finché l’umidità rimane sulle superfici. Quando si è verificata una macchia di stoccaggio bagnato, l’oggetto deve essere impilato per consentire alle superfici di asciugarsi rapidamente. Questo fermerà l’attacco e, con libero accesso all’aria, si formerà il normale strato protettivo. La macchia di stoccaggio a umido viene gradualmente lavata via e il rivestimento acquisisce un aspetto normale per l’acciaio zincato a caldo esposto.,
Poiché questo prodotto di corrosione bianca è molto ingombrante (circa 500 volte quello dello zinco da cui è stato formato), può sembrare serio. Tuttavia, la macchia di stoccaggio a umido ha spesso poca o nessuna importanza sulla durata della protezione contro la corrosione. Tuttavia, nel caso di rivestimenti molto sottili, ad esempio su oggetti elettrolitici, può essere significativo un grave attacco di macchia umida.
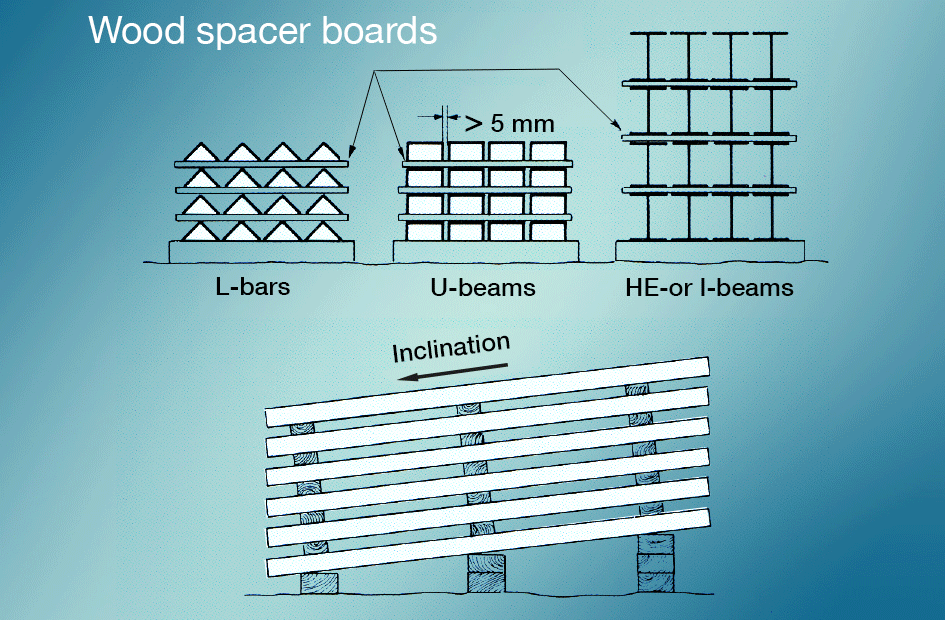
La macchia di stoccaggio a umido è meglio evitata impedendo alle superfici appena zincate di entrare in contatto con pioggia o condensa durante il trasporto., I materiali immagazzinati all’aperto devono essere impilati in modo che l’acqua possa fuoriuscire facilmente e in modo che tutte le superfici siano ben ventilate (fig. 5). La verniciatura dopo la zincatura offre un’ottima protezione.
Corrosione nel suolo
Le condizioni di corrosione nel suolo sono molto complicate e le variazioni possono essere grandi tra luoghi diversi, anche quelli in prossimità l’uno dell’altro. Il terreno può contenere prodotti alterati, sali liberi o legati, acidi e alcali, miscele di sostanze organiche, funghi ossidanti o riducenti,microrganismi ecc., A seconda della sua struttura, il terreno ha diversi gradi di permeabilità all’aria e all’umidità. Normalmente, il contenuto di ossigeno è inferiore a quello dell’aria, mentre il contenuto di anidride carbonica è più alto.
I terreni svedesi non sono generalmente molto aggressivi. La corrosione media per lo zinco è solitamente presa come 5 µm all’anno. Raramente si vedono terreni gravemente aggressivi. In Botnia nord e ovest, i suoli possono contenere zolfo. Sono spesso neri, ma si schiariscono quando esposti all’aria. In questi terreni, i tassi di corrosione dello zinco sono molto alti.
Un metodo per determinare la corrosività di un terreno è quello di misurare la sua resistività., Se la resitività del terreno non può essere determinata, le regole empiriche elencate nella figura 6 possono fornire una misura di orientamento. Per quanto riguarda l’esposizione dei metalli al suolo, tuttavia, è consigliabile rivolgersi a fonti qualificate.

la corrosione Galvanica

Se due metalli o leghe differenti, completamente o parzialmente circondati da un elettrolita, sono collegati, si crea una cella galvanica. Quale metallo diventa l’anodo o il catodo è determinato dai loro potenziali elettrodi nell’elettrolito in questione. Nell’acqua di mare, che corrisponde alla maggior parte delle condizioni pratiche, alcuni metalli e leghe occupano posizioni diverse sulla scala elettrochimica, mostrata in figura 7.,
Se l’acciaio è collegato al rame o all’ottone, l’acciaio diventa l’anodo nella cella e si corrode. Tuttavia, se l’acciaio è collegato al cadmio, all’alluminio, allo zinco o al magnesio, diventa il catodo ed è protetto dalla corrosione, mentre il metallo dell’anodo viene consumato. La corrosione galvanica è anche chiamata corrosione bimetallica e viene utilizzata per proteggere le strutture subacquee dalla corrosione, quando viene definita protezione catodica.
Protezione catodica garantita da rivestimenti in zinco
In acciaio zincato a caldo, zinco e acciaio sono in buon contatto elettrico tra loro., Se il rivestimento di zinco è danneggiato in presenza di un elettrolita viene creata una cella galvanica. L’elettrolita potrebbe essere condensa o acqua piovana. A volte l’intera struttura può essere immersa nel liquido. In questa cella lo zinco diventa l’anodo o il polo di dissoluzione, l’acciaio esposto diventa il catodo ed è quindi protetto dalla corrosione.
Nella fase iniziale è spesso possibile vedere una debole formazione di ust sulla parte esposta della superficie dell’acciaio dove il rivestimento è stato danneggiato, ma dopo un po ‘ si formano aree grigio-biancastre che si diffondono gradualmente su tutta l’area danneggiata., Il rivestimento di zinco corrode e le leghe di zinco scarsamente solubili scendono sulla superficie del catodo dove proteggono l’acciaio dal continuo attacco di ruggine. Questo è spesso chiamato “auto-guarigione”, che è qualcosa di un termine improprio dal momento che lo strato di zinco è, ovviamente, non ripristinato.
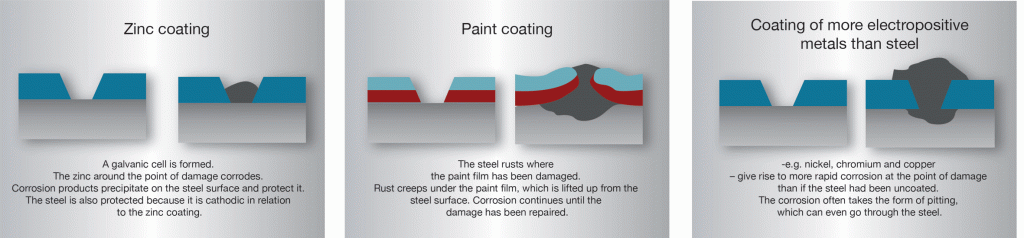
A causa della protezione catodica generata dallo zinco, la ruggine non può “insinuarsi” sotto il rivestimento nel punto di danno nel modo in cui può insinuarsi sotto film di vernice o rivestimenti di metalli più nobili dell’acciaio., I rivestimenti di zinco sull’acciaio sono insoliti, poiché un’area abbastanza ampia di danni al rivestimento non causa una perdita catastrofica di protezione dalla ruggine. La gamma di protezione catodica dipende dalla natura dell’elettrolita che crea la cellula. Per le strutture in atmosfere normali è normale prevedere un’azione protettiva di diversi millimetri. Tuttavia, in acqua di mare ci si può aspettare distanze significativamente maggiori.
Rivestimenti di zinco a contatto con metalli non ferrosi
La scala del potenziale elettrochimico mostra che lo zinco è meno nobile della maggior parte dei metalli comuni. Ciò significa che quando lo zinco è collegato a questi metalli in una cella galvanica è lo zinco che diventa il polo di dissoluzione. In linea di principio, pertanto, tali connessioni dovrebbero essere evitate quando possibile. Un buon metodo è quello di utilizzare un isolante come plastica o gomma al giunto.,
L’alluminio e l’acciaio inossidabile possono spesso essere collegati direttamente al materiale zincato in ambienti ariosi o abbastanza asciutti senza che si verifichi una corrosione evidente. Tuttavia, in acqua dovrebbe sempre essere usato un isolante.
Il rame e le leghe di rame sono più elettricamente attive e spesso c’è un rilascio di ioni di rame che si diffondono su grandi superfici e causano attacchi evidenti. Per questo motivo, questi metalli non dovrebbero mai entrare in contatto con l’acciaio zincato e dovrebbe essere utilizzato un isolante.,
Acciaio zincato a caldo a contatto con malta, intonaco e legno
Malta umida e intonaco attacco zinco. L’attacco cessa quando il materiale si asciuga. Il legno secco o moderatamente umido, sia impregnato che non impregnato, può essere inchiodato con chiodi zincati a caldo per un buon effetto. Tuttavia, nel caso di chiodi o raccordi filettati che sono costantemente esposti all’acqua, si preferisce un materiale resistente agli acidi. Altri materiali da costruzione secchi, come la lana minerale, non attaccano lo zinco.,
Imballaggio e trasporto di acciaio zincato
Anche se un rivestimento zincato a caldo è in grado di sopportare un trattamento abbastanza ruvido, deve essere maneggiato con cura durante lo stoccaggio e il trasporto. In caso di merci lunghe, l’imballaggio semplice e il legame in fasci non solo proteggono dai danni meccanici, ma spesso facilitano il trasporto stesso. Tuttavia, l’imballaggio e la rilegatura devono essere eseguiti in modo tale da evitare il rischio di deformazione da stoccaggio a umido. I distanziatori dovrebbero essere usati per prevenire tali attacchi.