1) Perdita di un occhio
Perdere un occhio per trauma, tumore o malattia oculare allo stadio terminale come glaucoma o diabete può essere devastante a qualsiasi età. Può avere un impatto importante sulla propria immagine di sé, fiducia in se stessi e autostima, per non parlare della regolazione necessaria per adattarsi alla visione monoculare (occhio singolo). Ci possono anche essere alcune restrizioni di lavoro che si applicano per i pazienti con un occhio solo (ad esempio, autisti commerciali, piloti di linea, poliziotti, vigili del fuoco, ecc.)., Numerosi pazienti sono stati dotati di occhi protesici che sono attualmente impiegati nelle professioni sopra menzionate. I pazienti monoculari dovrebbero cercare di tornare al loro lavoro se possibile e condurre una vita il più normale possibile. Anche se c’è una certa perdita di percezione della profondità e della visione periferica, non sono così “handicappati” come molti credono.
2) Procedure di presa primaria
a) Chirurgia di enucleazione – L’enucleazione si riferisce alla rimozione del globo (bulbo oculare)., La chirurgia può essere eseguita in anestesia locale stand-by (anestesia crepuscolare) o in anestesia generale (paziente addormentato). È comunemente fatto come paziente ambulatoriale o durante la notte. La procedura chirurgica richiede generalmente circa 1 ora. Durante l’anestesia, i coperchi sono tenuti aperti e gli strati esterni dell’occhio (congiuntiva e tenoni) sono tagliati lontano dal bulbo oculare. Anche i muscoli extraoculari (responsabili dello spostamento dell’occhio in diversi campi dello sguardo) vengono tagliati lontano dalla superficie dell’occhio. Infine il nervo ottico viene tagliato e l’intero bulbo oculare viene rimosso., Il sanguinamento è controllato da cauterizzazione delicata.

Figura 1: Esempi di impianti orbitali negli ultimi 20 anni (lato destro della foto) e occhi artificiali (lato sinistro della foto).
Quando qualcuno perde un occhio, sono necessari due componenti: un impianto orbitale per mantenere il volume della cavità oculare e un occhio artificiale o una protesi.
Quindi, dopo la rimozione dell’occhio, un impianto orbitale viene inserito nella presa e i tessuti vengono chiusi sopra di esso., I muscoli extraoculari possono essere collegati alla superficie dell’impianto per aiutare a mantenere l’impianto dalla migrazione e per aiutare con il movimento della presa. Inizialmente, un conformatore protesico temporaneo in plastica trasparente viene posto sopra l’impianto orbitale. Questo conformatore mantiene lo spazio del tessuto dietro le palpebre dove l’occhio protesico alla fine siederà. In circa 6-8 settimane, il conformatore viene rimosso e un occhio artificiale su misura (protesi) è fatto per la presa. Collirio o unguento sono necessari durante le prime settimane post-operatorio., Il dolore è qualcosa di cui i pazienti si preoccupano abitualmente con la chirurgia di enucleazione. Ci può essere qualche disagio post-operatorio nei primi giorni, ma quanto è variabile, come ognuno ha una soglia di dolore diverso. Quello che potrebbe essere un sacco di dolore per una persona può essere solo lieve a moderata in un altro. Qualunque sia il dolore presente (di solito non grave) si attenua nei primi 3-5 giorni. Gli antidolorifici vengono regolarmente prescritti dopo l’intervento chirurgico di enucleazione insieme agli antibiotici.,
b) Chirurgia di eviscerazione-La chirurgia di eviscerazione si riferisce alla rimozione del contenuto interno dell’occhio (cornea, iride, lente, vitreo e retina). Il guscio bianco dell’occhio (sclera) è lasciato in posizione. I muscoli extraoculari sono lasciati attaccati alla superficie dell’occhio e il nervo ottico non viene tagliato. Una volta rimosso il contenuto dell’occhio, un impianto viene inserito nel guscio sclerale. La sclera, i tenoni e la congiuntiva vengono quindi chiusi sull’impianto e viene messo in atto un conformatore temporaneo (plastica trasparente)., Il vero occhio artificiale (protesi) viene realizzato in circa 6-8 settimane.
L’eviscerazione, come l’enucleazione, può essere eseguita in stand-by locale (anestesia crepuscolare) o in anestesia generale e può essere eseguita in regime ambulatoriale o come visita di pernottamento. Come l’enucleazione, il dolore è variabile e dipende dalla soglia del dolore. Generalmente, c’è qualche dolore, ma di solito non è grave. Si deposita nei primi 3-5 giorni.

Figura 2a: Occhio destro cieco, doloroso, sfigurato con evidente cicatrice.,
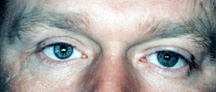
Figura 2b: Dopo l’intervento di eviscerazione e la revisione della cicatrice.
Qual è il migliore: enucleazione o eviscerazione? Eviscerazione è più veloce e più semplice da fare. C’è meno rottura anatomica alla cavità oculare con eviscerazione e i risultati finali (aspetto, movimento) sono superiori nella maggior parte dei casi con l’enucleazione. Tuttavia, ci sono alcune situazioni in cui semplicemente non si può avere un’eviscerazione. In qualsiasi occhio che ha un tumore (ad esempio, melanoma) o tumore sospetto, un’enucleazione è l’unica opzione., Se l’occhio malato ha glaucoma allo stadio terminale, diabete allo stadio terminale, è un occhio post trauma, ha una storia nota senza sospetto di un tumore, un’eviscerazione è adatta e diventa sempre più comune a causa della facilità dell’intervento chirurgico e degli eccellenti risultati cosmetici (Figura 2a, b).
c) Chirurgia implantare orbitale secondaria – In alcuni individui che avevano precedentemente avuto una procedura di enucleazione anni fa, l’impianto orbitale potrebbe essersi spostato fuori posizione, essere esposto, infetto o semplicemente troppo piccolo., In questa situazione è possibile eseguire un intervento chirurgico secondario per rimuovere il primo impianto (chirurgia implantare orbitale secondaria). La chirurgia implantare orbitale secondaria può essere più impegnativa dell’enucleazione o dell’eviscerazione, specialmente se il chirurgo cerca di localizzare e ricollegare i muscoli extraoculari. Pertanto, di solito viene eseguito in anestesia generale come paziente durante la notte. La guarigione post-operatoria è simile alla chirurgia di enucleazione ed eviscerazione.,
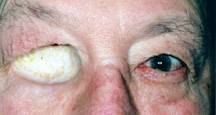
Figura 3a: Presa di Exenteration (un innesto cutaneo che appare molto più leggero della pelle circostante sta rivestendo la cavità oculare).
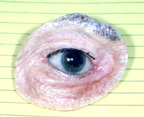
Figura 3b: Protesi oculo-facciale

Figura 3c: La protesi oculo-facciale si trova nella cavità oculare. Gli occhiali camoflauge la protesi
d) Chirurgia di Exenteration – Exenteration è una procedura più radicale di enucleazione, eviscerazione o impianto orbitale secondario., Comporta la rimozione di tutti i tessuti all’interno dell’intera cavità oculare. La congiuntiva, il globo, i muscoli extraoculari e il grasso orbitale sono tutti eliminati. In queste situazioni non c’è posto per mettere un impianto orbitale o un occhio artificiale come descritto sopra. Una protesi oculo-facciale può essere fatta tuttavia, per coprire l’apertura della cavità oculare. Sebbene non si muova, sembra molto meglio di una cavità oculare vuota (Figura 3a, b,c).
3) Impianti orbitali
Prima del 1885 non venivano utilizzati impianti orbitali., L’occhio è stato rimosso dall’enucleazione o dall’eviscerazione e la presa è stata lasciata per guarire da sola. Il risultato fu un’antiestetica depressione sommersa delle palpebre nella cavità oculare. L’uso di un impianto orbitale è stato un importante passo avanti nella chirurgia della presa anoftalmica. L’impianto ha migliorato la cosmesi postoperatoria riempiendo il volume orbitale e riducendo anche la possibilità di contrazioni della presa a causa della formazione di tessuto cicatriziale., Negli ultimi 100 anni sono stati utilizzati vari materiali per l’impianto orbitale, tra cui: oro, argento, cartilagine, osso, grasso, sughero, spugna, gomma, paraffina, lana, amianto, così come una varietà di altri nel tentativo di trovare l’impianto più biocompatibile (Figura 1).
Una varietà di forme e dimensioni sono state anche provate nel tentativo di promuovere una certa motilità al socket. Nel 1985 un nuovo concetto di protesi oculare ha cominciato ad evolversi quando un ricercatore (Dr. Arthur Perry, San Diego, CA) ha iniziato a studiare il corallo del mare come un impianto oculare., Attraverso un processo idrotermale brevettato, la componente di carbonato di calcio del corallo marino è stata trasformata in fosfato di calcio ed è stata prodotta una sostanza nota come idrossiapatite. L’idrossiapatite ha la stessa struttura chimica e la stessa struttura porosa del tessuto osseo umano (Figura 4a).

Figura 4a: Idrossiapatite orbitale impianto
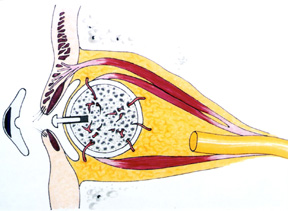
Figura 4b: Disegno di idrossiapatite impianto con muscoli collegati, e un peg in posizione

la Figura 4c: idrossiapatite Sintetica dell’impianto.,

Figura 4d: Polietilene sferico poroso.
Il materiale implantare (idrossiapatite corrallina) è biocompatibile, atossico e anallergico. Il tessuto del corpo riconosce il materiale come simile e, a causa della natura porosa, il tessuto crescerà in esso. L’impianto diventa più fisso e quindi resiste alla migrazione. L’impianto consente il fissaggio dei muscoli extraoculari che a sua volta porta a una migliore motilità dell’impianto orbitale., L’impianto orbitale può anche essere collegato direttamente alla protesi attraverso un piolo, sporgente dall’impianto (Figura 4b) consentendo un’ampia gamma di movimenti protesici e i movimenti oculari guizzanti comunemente osservati quando le persone sono impegnate in una conversazione. La gamma aumentata e i movimenti darting fini permettono una qualità più vitale all’occhio protesico.
L’impianto di idrossiapatite, noto anche come Bio-Eye™ (integrated Orbital implants, San Diego) è chiamato “impianto poroso.”Dalla sua introduzione, sono stati introdotti una serie di altri “impianti porosi”., Uno di questi impianti (reso popolare dal Dr. D. R. Jordan-University of Ottawa Eye Institute, Ottawa, Ontario, Canada) è una varietà sintetica di idrossiapatite (impianto FCI3 HA) che ha qualità simili all’originale Bio-Eye™ ma meno costoso (Figura 4c). E ‘ disponibile in Canada e in altre parti del mondo, ma a causa di restrizioni di brevetto non è disponibile negli Stati Uniti. Un altro impianto poroso sintetico che è diventato sempre più popolare è un tipo di plastica porosa noto come polietilene poroso (Medpor™ – Porex Surgical Inc, Cooledge Park, GA)., Questo materiale è un materiale sintetico artificiale che in precedenza è stato utilizzato in una vasta gamma di procedure ricostruttive cranio-facciali e fratture facciali, con pochi problemi. Le sue proprietà dimostrano elevata resistenza alla trazione, malleabilità, biocompatibilità e crescita fibrovascolare. Gli impianti orbitali in polietilene poroso sono anche più economici dell’originale Bio-Eye™ e sono disponibili in forme sferiche, a uovo, coniche o montate (Figura 4d).,
Ossido di alluminio (Al2O3) un altro biomateriale artificiale che è stato in uso per più di 30 anni come impianto in ortopedia e odontoiatria è stato anche ampiamente studiato (Dr. D. R. Jordan-University of Ottawa Eye Institute, Ottawa, Ontario, Canada) e sta emergendo come impianto orbitale in Canada, Europa e molte altre parti del mondo. L’impianto di ossido di alluminio, noto anche come impianto bioceramico (FCI, Issy-Les-Moulineaux, Cedex, Francia) sembra identico all’idrossiapatite Bio-Eye™ con pori multipli interconnessi., Come l’HA sintetico e il polietilene poroso, è meno costoso del Bio-Eye™. Ci sono prove che osteoblasti e fibroblasti umani sembrano crescere meglio sull’ossido di alluminio rispetto all’idrossiapatite, suggerendo che potrebbe essere più biocompatibile dell’idrossiapatite e meglio tollerato nella cavità oculare.1,2,3
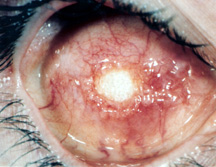
Figura 5a: Esposizione di un impianto di idrossiapatite.,
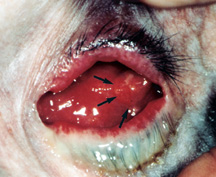
Figura 5b: Infezione dell’impianto orbitale – la cavità oculare è molto infiammata, c’è molta scarica e un granuloma piogenico ricorrente (frecce nere).
4) Complicanze dell’impianto orbitale
Le complicanze associate all’idrossiapatite che si applicano anche ad altri impianti orbitali porosi sono gradualmente venute alla luce dall’introduzione e dall’uso diffuso dell’idrossiapatite nei primi anni 1990., Le complicanze riportate includono: esposizione all’impianto, assottigliamento congiuntivale, scarico, formazione di granuloma piogenico (formazione di tessuto cicatrizzante in eccesso) e raramente dolore o disagio persistente. La complicazione discussa più spesso è l’esposizione all’impianto con tassi di esposizione che vanno dallo 0 al 22% (Figura 5a).,
I fattori predisponenti all’esposizione includono: chiusura della ferita sotto tensione, tecnica di chiusura della ferita inadeguata o scadente, infezione, irritazione meccanica o infiammatoria dalla superficie speculata dell’impianto HA e crescita ritardata del tessuto fibrovascolare con successiva rottura del tessuto.
La complicanza più temuta degli impianti orbitali porosi è l’infezione all’interno dell’impianto., Gli impianti orbitali porosi hanno pori interconnessi multipli che si riempiono di tessuto fibrovascolare nei primi 6-12 mesi che teoricamente dovrebbero aiutare a resistere alle infezioni. Prima di questo tempo l’esposizione dell’impianto può predisporre l’impianto all’ingresso di contaminazione batterica e infezione dell’impianto. Una volta che si verifica un’infezione implantare, potrebbe non essere facile da riconoscere o trattare. Caratteristiche dell’infezione dell’impianto sono: scarico ricorrente resistente a più gocce, disagio dell’impianto (al tatto) e granuloma piogenico ricorrente (eccesso di tessuto curativo) sulla superficie dell’impianto (Figura 5b).,
L’infezione implantare non risponde agli antibiotici orali, endovenosi e / o topici e generalmente l’impianto deve essere rimosso. La rimozione di un impianto infetto richiede un’anestesia generale ed è traumatica per l’orbita oculare poiché l’impianto è stato parzialmente integrato con il tessuto dell’orbita. Dopo la rimozione dell’impianto orbitale poroso non è consigliabile avere un altro impianto poroso fino a quando non sia trascorso un periodo di tempo sufficiente (almeno 6 mesi) per garantire la guarigione dei tessuti., Una sfera non porosa di plastica può essere inserita per mantenere il volume mentre aspetta il periodo di 6 mesi e contempla un altro impianto poroso.
5) Motilità dell’occhio artificiale: Procedure di Pegging dell’impianto
a) Per peg o non per peg? Uno dei tanti vantaggi degli impianti porosi (idrossiapatite, polietilene poroso, ossido di alluminio) è la capacità di integrarli con l’occhio artificiale sovrastante attraverso un sistema di peg., Accoppiando l’impianto orbitale all’occhio artificiale può verificarsi una vasta gamma di movimenti oculari protesici e movimenti oculari guizzanti comunemente visti nel discorso conversazionale. Questi movimenti conferiscono una qualità più vitale all’occhio protesico. Peg o non peg, spetta al chirurgo e al paziente. Essi non sono certamente per tutti e con tutto il dovuto rispetto, non tutti i chirurghi cavità oculare sono ugualmente abili a metterli in., Prima di considerare un piolo l’impianto deve essere completamente vascolarizzato (minimo di 6 mesi, in alcuni questo può richiedere un anno o più) e, la presa deve essere uno sano. I pazienti con diabete, radiazioni precedenti, malattie sistemiche come il Lupus eritematoso sistemico (LES) o, individui su farmaci come gli steroidi, non sono buoni candidati per il pegging, perché il loro tessuto socket semplicemente non ha un buon flusso sanguigno.
I pioli non sono infallibili e hanno un proprio insieme intrinseco di problemi al di là di quelli dell’impianto., Per ottenere ottimi risultati è necessaria una meticolosa tecnica di peg placement; un fatto non apprezzato da molti. I pioli devono essere centrali e dritti. Devono anche essere a filo con l’impianto senza porzione esposta per garantire un buon risultato. Una volta ancorato, gli individui richiedono un follow-up regolare inizialmente per essere sicuri che il piolo è seduto bene. Con il tempo i follow-up possono diminuire (annualmente) se tutto va bene. Il problema più preoccupante associato al pegging è l’introduzione di infezione all’impianto, che richiede la rimozione dell’impianto.,
Altri potenziali problemi di peg includono scarico, granuloma piogenico (tessuto curativo in eccesso) attorno al piolo, caduta del piolo, scarso trasferimento di movimento, clic, crescita eccessiva congiuntivale, scarsa vestibilità o manicotto allentato, parte dell’albero del manicotto visibile, peg forato su un angolo, peg forato del centro, HA visibile attorno al foro del piolo e movimento

Figura 6a: Sistema di peg in policarbonato – il peg standard originale è a destra (freccia nera); il peg e il sistema di maniche a sinistra con cacciavite per il manicotto sottostante.,

Figura 6b: peg titanio puro e sistema manica.

Figura 6c: Manicotto in titanio rivestito di idrossiapatite con diversi pioli in titanio.
Così, anche se pioli consentono una qualità più realistica per l’occhio artificiale, non sono per tutti.
b) Variazioni Peg (Figura 6a)
il peg originale era in plastica (policarbonato). Un foro è stato praticato nell’impianto e un piolo standard è stato messo in atto., Per ottenere una vestibilità più sicura tra l’impianto orbitale e il peg, è stato progettato un sistema di peg e sleeve. Dopo la perforazione di un foro nell’impianto, un manicotto viene avvitato nell’impianto fino a quando non è stretto e a filo con la superficie dell’impianto. Un piolo viene quindi posizionato al centro della manica. Negli anni più recenti il titanio ha sostituito il policarbonato come materiale per piolo e manicotto poiché è meglio tollerato nel tessuto dell’incavo(più biocompatibile).,
Alcune aziende producono sistemi di peg in titanio puro (Figura 6b) mentre altre producono titanio rivestito di idrossiapatite (Figura 6c).
Il rivestimento in idrossiapatite si traduce in una resistenza dell’interfaccia significativamente maggiore rispetto al titanio non rivestito.
6) Procedure ricostruttive Socket
a) Aumento del volume-un certo grado di affondamento è comune nei pazienti con occhio artificiale., La scelta appropriata di un’adeguata dimensione dell’impianto al momento dell’enucleazione o dell’eviscerazione è il primo passo per ridurre l’aspetto sommerso del paziente con occhio artificiale. Tuttavia, se rimane qualche affondamento, sono disponibili tecniche per diminuirlo. Un’opzione è quella di sottoporsi a una seconda procedura chirurgica per impiantare un secondo impianto (impianto a slitta o a pavimento) nella cavità oculare, sotto e dietro il primo. Un anestetico generale è richiesto per mettere questi impianti di aumento del volume nella posizione. Sono progettati per scivolare sotto e posteriormente al primo impianto., Possono essere fissati in posizione da colla, filo o un sistema di mini piastra utilizzato nella ricostruzione facciale. L’intervento è breve (45 minuti) e i pazienti vengono dimessi con un cerotto sul posto il giorno dell’intervento o la mattina successiva. L’occhio artificiale rimane in posizione, ma può richiedere un aggiustamento nelle prime settimane. Il dolore non è un fattore importante in quanto vi è una minima interruzione dei tessuti del socket (Figura 7a,b).
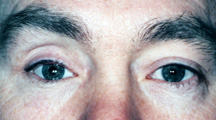
Figura 7a: Aspetto socket affondato.,
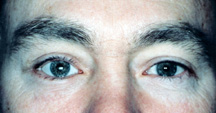
Figura 7b: 3 mesi dopo un impianto di pavimento orbitale – l’aspetto affondato è scomparso.
Un’altra tecnica per ridurre un aspetto affondato prevede l’uso di innesti di “grasso cutaneo”. Un innesto di grasso appena sotto la pelle (”grasso dermico”) può essere raccolto dall’anca del paziente. Questo grasso viene poi impiantato nel coperchio superiore che appare affondata (solco). L’incisione dell’anca si trova sotto l’area della biancheria intima o del costume da bagno., Il grasso viene tagliato e impiantato nel coperchio superiore (solco) che appare incavato, facendo un’incisione della piega della pelle delle palpebre lunga 1 pollice. Una tasca è fatta per l’innesto grasso, che viene poi impiantato seguito da chiusura della pelle. Questa procedura viene eseguita di routine in anestesia locale o locale in stand-by (anestesia crepuscolare) come paziente diurno. Non è doloroso e ha risultati da buoni a eccellenti. È necessaria una correzione eccessiva poiché nei primi 3 mesi si verifica un’atrofia grassa.,
Infine, per bilanciare l’aspetto sommerso dell’occhio artificiale, è possibile eseguire la rimozione di una piccola quantità di pelle e grasso dal coperchio superiore dell’occhio vedente opposto. Questa è una procedura molto semplice e veloce che viene eseguita di routine come ambulatoriale. A volte può essere eseguito con buoni risultati anche prima della considerazione degli” impianti a pavimento “o della” tecnica di innesto di grasso” descritta.,
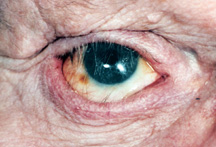
Figura 8: Con un fornice inferiore poco profondo il coperchio inferiore appare spinto verso il basso e le ciglia vengono arrotolate verso l’alto verso la protesi.
b) Ricostruzione del fornice – Dopo molti anni di indossare un occhio artificiale, infezione ricorrente della presa e / o cicatrici secondarie al trauma, la tasca dietro il coperchio inferiore dove si trova l’occhio artificiale (“fornice inferiore”) può diventare superficiale., Ciò può essere associato a un coperchio inferiore retratto (un coperchio inferiore che sembra troppo basso) e problemi di adattamento dell’occhio artificiale con la caduta ricorrente dell’occhio artificiale (Figura 8).
Per correggere questo, una valutazione iniziale da parte dell’oculista può essere eseguita per determinare se una protesi modificata su misura potrebbe essere di qualche beneficio. In caso contrario, è necessaria una procedura chirurgica di approfondimento del fornice. Uno di questi interventi consiste nel prendere in prestito parte del rivestimento dall’interno della bocca (membrana mucosa) e usarlo per creare una tasca del coperchio inferiore più profonda., La mucosa del palato duro (dal palato della bocca) può anche essere usata come pure cartilagine dell’orecchio o sclera del donatore. Questi interventi vengono eseguiti in anestesia locale stand-by (anestesia crepuscolare) o in anestesia generale. Generalmente richiedono 1-1½ ore e sono molto ben tollerati. Se si utilizza la mucosa del palato duro, cibi caldi e liquidi possono essere difficili da tollerare per alcune settimane.
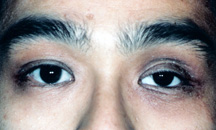
Figura 9: Abbassamento del coperchio superiore sinistro.,
7) Chirurgia ricostruttiva delle palpebre
a) Ptosi del coperchio superiore – ptosi si riferisce a “cadenti.”Un coperchio superiore cadente o” coperchio superiore ptotico ” non è raro. Dopo diversi anni di indossare un occhio artificiale e rimuoverlo in numerose occasioni, è possibile che il muscolo di elevazione del coperchio superiore (aponeurosi del levatore) diventi sottile e si allunghi. Di conseguenza, il coperchio superiore cade e diventa “ptotico” (Figura 9).
Se la caduta del coperchio è lieve, una regolazione dell’occhio artificiale può elevare il coperchio e correggere la caduta., Se il coperchio rimane cadente, è possibile eseguire un’operazione semplice, rapida e indolore denominata “levator advancement”.”L’intervento richiede circa 15-30 minuti e viene eseguito sotto congelamento locale come ambulatoriale. Post-operatoria ci possono essere alcuni piccoli lividi e gonfiore nella prima settimana.
b) Lassità del coperchio inferiore-Dopo molti anni di indossare un occhio artificiale, il coperchio inferiore (che supporta il peso dell’occhio artificiale) può diventare lassista (sciolto). Di conseguenza, i cali inferiori verso il basso. Per correggere questo, è possibile eseguire una procedura di serraggio del coperchio minore., In anestesia locale come ambulatoriale, viene effettuato un snip nella parte laterale del coperchio e la parte ferma del coperchio (piastra tarsale) viene ricollegata al bordo orbitale osseo. Questa procedura, comunemente indicata come “striscia tarsale” è semplice da fare. Ci vogliono circa 15 minuti e relativamente senza dolore. Le suture utilizzate sono dissolvibili e solo raramente causano una certa tenerezza durante l’assorbimento.
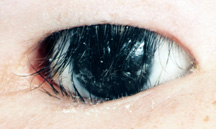
Figura 10: Entropione delle palpebre superiore e inferiore – notare le ciglia appoggiate sulla superficie della protesi.,
c) Entropion repair – Entropion si riferisce ad una rotazione verso l’interno del coperchio (Figura 10). Nel paziente con occhio artificiale può essere visto sul coperchio superiore e inferiore. Quando si verifica l’entropione, le ciglia diventano più verticali nel coperchio superiore e inferiore e possono finire appoggiate sull’occhio protesico. La chirurgia per l’entropione del coperchio superiore o inferiore è disponibile, generalmente come ambulatoriale in anestesia locale. Gli interventi chirurgici di solito durano 30 minuti e l’obiettivo è quello di ruotare le ciglia nel coperchio superiore o inferiore in una posizione più normale., Le suture utilizzate sono assorbibili e si dissolvono in 3-6 settimane a seconda del tipo utilizzato. Post-operatorio ci possono essere lievi gonfiore e lividi. Il dolore non è una grande preoccupazione, ma qualche disagio minore può essere presente.
d) Ectropion repair-Ectropion si riferisce ad una rotazione verso l’esterno del coperchio inferiore. Dopo diversi anni di usura dell’occhio artificiale e sviluppo di lassità tissutale nel coperchio inferiore, il coperchio inferiore non solo può abbassarsi verso il basso ma può, in alcuni casi, allontanarsi dall’occhio artificiale (diventare ectropico)., Come l’entropion, questo problema può essere corretto con una procedura ambulatoriale molto semplice in anestesia locale con suture assorbibili. L’obiettivo è riportare la palpebra in una posizione più normale in modo che si trovi contro l’occhio artificiale. La chirurgia dura 15-30 minuti e può essere associata a qualche piccolo gonfiore del coperchio e lividi.
8) Osservazioni conclusive sugli occhi artificiali
Il contatto visivo è una parte essenziale dell’interazione umana. È estremamente importante che il paziente con occhio artificiale mantenga un occhio protesico naturale e normale., Negli ultimi anni si sono verificati importanti sviluppi nella ricostruzione di una cavità oculare dopo enucleazione/eviscerazione o chirurgia implantare secondaria. L’impianto orbitale ideale è stato ricercato per più di un secolo. I materiali porosi (idrossiapatite, polietilene poroso e ossido di alluminio) sono attualmente gli impianti orbitali preferiti principalmente a causa della vascolarizzazione e dell’integrazione tissutale che possono verificarsi., Questi impianti hanno meno probabilità di migrare rispetto all’impianto di plastica utilizzato in precedenza e sono associati a un più alto grado di motilità, specialmente se accoppiati all’occhio artificiale sovrastante attraverso un sistema di peg. Quale impianto è migliore è attualmente una questione di dibattito. L’impianto poroso ideale è quello biocompatibile, bioinerte, atossico, anallergico, economico e stabile nel tempo.
1. Labat B. Chanson A., Frey J. Effetti dei rivestimenti di allumina e idrossiapatite nella crescita e nel metabolismo degli osteoblasti umani., J Biomed Mater Res 1995; 29:1397-1401
2. Mawn L, Jordan DR, Ahmad I, Gilberg S. Effetti dei biomateriali orbitali sui fibroblasti umani. Can J Ophthalmol 2001; 36: 245-251
3. Christel P. Biocompatibilità dell’allumina policristallina densa di grado chirurgico.Clin Orthop 1992; 282: 10-18