Nonvalvular fibrilace síní (NVAF) je nejčastěji se vyskytující arytmií v Španělsko. Incidence úzce souvisí s věkem, s prevalencí téměř 25% u pacientů starších 80 let.1 mezi mnoha procesy spojenými s NVAF je cerebrovaskulární příhoda kardioembolického původu pravděpodobně nejzávažnější komplikací, protože vede k vysoké míře postižení a úmrtnosti.,2 Dalším problémem spojeným s fibrilací síní je potřeba perorální antikoagulační (OAC) terapie k prevenci kardioembolických příhod. Tato potřeba roste s pokročilým věkem, protože riziko události je ještě větší.1 u těchto pacientů se navíc zvyšuje riziko komplikací spojených s antikoagulační terapií, zejména krvácení.3 v současné době je okluze perkutánní levé síně (LAA) alternativou pro pacienty s nvaf a kontraindikací léčby OAC.,4,5
perorální antikoagulační terapie: účinnost a omezení
antikoagulační léčba antagonisty vitaminu K je považována za standardní léčbu NVAF. Hlavními problémy s těmito léky jsou zvýšené riziko krvácení, potřeba pravidelných kontrol, interakce s jídlem nebo jinými léky a nestabilita účinku léků v některých případech. Odhaduje se, že mezi 30% a 50% pacientů indikovaných pro OAC je nedostává.6 se zavedením nových antikoagulancií, jako je dabigatran, 7 apixaban, 8 a rivaroxaban, by se mohlo změnit 9 řízení těchto pacientů., Ať už může být případ, a to i přes jejich více stabilní a bezpečnější akční profil, riziko krvácení, s roční sazbou mezi 2,1% a 3,6%, nadále bude hlavní Achillovou patou těchto nových látek (Tabulka). Ve skutečnosti novější registry naznačují, že výskyt kardioembolických příhod a krvácení sekundární k dabigatranu by mohl být podobný výskytu warfarinu.10 i Přes zavedení nové antikoagulační činidla, procento pacientů indikován pro OAC ale ne léčby zůstává kolem 40%.,11 Potýkají se špatným dodržování léčby a přetrvávající riziko krvácení, potřebu alternativy k antikoagulační terapie se stala prioritou pro tyto pacienty.
přívěsek levé síně: funkce, anatomie a indikace pro okluzi
LAA je embryologický zbytek a jeho hlavní funkcí je kontrola objemu krve. Nachází se velmi blízko levé circumflexní tepny, hraničící v horní úrovni s levou horní plicní žílou a na spodní úrovni s mitrální chlopní., Morfologie LAA je mimořádně heterogenní od jednoho pacienta k druhému a často existuje více než jeden lalok. V sinusovém rytmu je LAA kontraktilní struktura, která vyprázdňuje jeho obsah při každém srdečním tepu. Při fibrilaci síní ztrácí LAA kontraktilní kapacitu a rozšiřuje se, což vede ke zpomalení průtoku krve, s následným zvýšeným rizikem trombózy. V patologických studiích pacientů s NVAF se v LAA nachází 91% trombů umístěných v levé síni., To vedlo k přesvědčení, že perkutánní Laa okluze může být účinnou strategií k prevenci kardioembolického rizika u pacientů s NVAF.
perkutánní Laa okluze je stále v počáteční fázi a ještě několik let musí projít, než můžeme získat spolehlivější pohled na její roli u pacientů s NVAF. I když v budoucnu může představovat skutečnou alternativu pro pacienty bez kontraindikací OAC, v současné době by jeho použití mělo být vyhrazeno pacientům s kontraindikacemi antikoagulační terapie, jak je doporučeno v evropských pokynech (indikace IIb).,5 Ve skutečnosti, většina postupů u pacientů užívajících antikoagulační terapii jsou uvedené buď neurologie služby po epizodě intrakraniální krvácení, nebo gastroenterologie následující pozorování opakující se zažívací krvácení bez léčitelné příčiny. Nedostatek platné alternativy k OAC, aby se zabránilo cardioembolic riziko, které je obecně vysoká, protože tyto jsou obvykle starší pacienty s více patologiemi, aby okluze LAA velmi atraktivní možností pro tyto pacienty., Labilní mezinárodní normalizovaný poměr nebo vzhled cardioembolic událost i přes OAC zacházení a odpovídající mezinárodní normalizovaný poměr jsou jiné kontexty, v nichž perkutánní okluze LAA by mohla být oprávněná. V každém případě, multidisciplinární, individuální rozhodnutí jsou potřebné k posouzení obou cardioembolic a riziko krvácení a další důležité faktory, jako je účinnost léčby, křehkost pacienta, nebo dodržování léčby, zejména s OAC.
perkutánní zařízení pro okluzi levé síně
zařízení PLAATO™ bylo prvním perkutánním occluderem LAA(obr. 1)., Navzdory dobrým předběžným výsledkům z hlediska účinnosti a bezpečnosti byl vývojový program pozastaven a zařízení zmizelo z trhu.
v Současné době, obě zařízení se nejčastěji používá po celém světě jsou Hlídač™ systém (Boston Scientific; Boston, Massachusetts, Spojené Státy) a Amplatzer™ Cardiac Plug (AKT) (St. Jude Medical; Minneapolis, Minnesota, Spojené Státy) (Obr. 1). Stejně jako systém PLAATO™ jsou obě implantovány transseptální cestou pomocí přístupu femorální žíly., Obě protézy jsou vysoce flexibilní a mají systém stabilizace vodicích drátů, že kotva do LAA zeď, a vyhnout se embolizaci. Hlavní rozdíl mezi oběma zařízeními je však v jejich tvaru. Hlídač™ systém je implantován v 10 mm od LAA ústí, a proto není kryt; AKT obsahuje laloku, který je implantován 10-15 mm od ústí a disk, který zcela pokrývá LAA ústí (Obr. 2). Druhá generace ACP s názvem Amplatzer ™ Amulet™ se nedávno objevila na trhu. Zařízení Amulet™ (obr., 1) je také ve tvaru laloku a má disk jako akt, ale má modifikace, které usnadňují přípravu a implantaci zařízení a současně minimalizují riziko embolizace a trombózy.
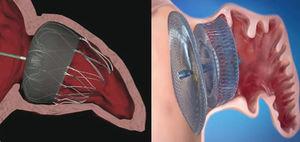
poloha zařízení se srdeční zástrčkou Watchman™ a Amplatzer™ po implantaci do levé síně., Hlídač™ zařízení implantované v 10 mm od ústí z levé sine přívěsku (vlevo) a Amplatzer™ Cardiac Plug zařízení s laloku implantované v 10 mm od ústí a disk pokrývající vstup do ouška levé síně (vpravo).
Četné registrů svědčí o účinnosti a bezpečnosti Hlídač™ systému a AKT, ale oba vyžadují ne-zanedbatelný implantace křivka učení., PROTECT AF studie,12 pouze randomizované studii porovnat warfarin s LAA okluze (Hlídač™) u pacientů s NVAF, ukázal, že okluze LAA je ne méně úspěšný než warfarin o primární cíl (kombinované cévní mozková příhoda, systémová embolizace a kardiovaskulární nebo nevysvětlitelné smrti), ale ukázal znepokojující mírou periprocedural události, s 4.4% výskyt závažné perikardiální výpotek., Tento počáteční problém byl přičítán křivce učení operátora: se zkušenostmi operátora klesla míra komplikací a procento úspěšných implantací se výrazně zlepšilo. V současné době (pro obě zařízení) více než 95% implantátů jsou obecně úspěšné a silné perikardiální výpotek sazba je
TECHNICKÉ ÚVAHY
perkutánní okluze LAA technika vyžaduje tým se zkušenostmi v vrozené/strukturální onemocnění., I když některé skupiny používají pouze intrakardiální echokardiografie, nebo i angiografické kontroly, k vedení řízení a vyhnout se pacienta intubace, většina center pomocí transezofageální echokardiografie (TEE) v celkové anestezii. Strukturálně má LAA velmi jemné stěny a heterogenní morfologii, která může skrýt mikrotrombózy z odpaliště. Zkušenosti s operátorem jsou nezbytné pro minimalizaci manipulace v LAA a tím snížení rizika perforace a periprocedurální embolie., Dva z nejdůležitějších faktorů, které minimalizují manipulaci v LAA jsou následující: a) nízké zadní transseptal defekt, který usnadňuje čelní přístup do LAA, a b) podrobnou studii LAA, pokud je to možné s TEE a angiografie, s cílem vytvořit LAA morfologie a získat přesné opatření, která usnadní výběr velikost okluderu. Doporučuje se provádět měření při normálním objemu krve, protože velikost LAA se může významně lišit jako funkce úrovně hydratace pacienta., V průběhu řízení, pacienti mají tendenci, aby se stal dehydrataci, a proto, je doporučeno, že levé síně tlak být stanovena a tekuté podáván k udržení >10 mmHg tlak, než začnete měření.
jedná se o relativně nový postup a přestože TEE je zobrazovací standard, ideální zobrazovací režim zůstává neznámý. Morfologie LAA je oválná u 80% pacientů, takže průměry se obvykle liší kvůli krátkým a dlouhým osám. Tento rozdíl může zůstat bez povšimnutí pomocí 2-dimenzionálních zobrazovacích technik., Stejně jako v postupech, jako je náhrada perkutánní aortální chlopně, může 3-dimenzionální TEE nebo srdeční tomografie poskytnout prostorové informace, které mohou pomoci optimalizovat implantační strategii a výběr velikosti zařízení.
význam periprotézních úniků během sledování zůstává nejistý. Studie PROTECT Af subanalýza nezjistila žádný vztah mezi úniky a výskytem klinických příhod., Naproti tomu ve studiích výsledků koronární srdeční chirurgie byla neúplná excize LAA u pacientů, kteří měli chirurgickou profylaktickou Laa okluzi, spojena s vyšší mírou kardioembolických příhod. Když čekáme, až budou k dispozici nové studie, které mohou nebo nemusí tento vztah potvrdit, měli bychom se pokusit zabránit periprotézním únikům. Proto se doporučuje, aby zařízení bylo o něco větší než TEE a angiografická opatření by naznačovala, protože to umožňuje snížit rychlost zbytkových úniků bez zvýšení rizika prasknutí stěny LAA.,13
Postprocedurální antitrombotická doporučení jsou dalším kontroverzním problémem. Ve studii PROTECT AF byl OAC podáván po dobu 45 dnů postimplantation a pozastaven, pokud TEE vykazoval odpovídající Laa okluzi.12 nedávno studie ASAP ukázala, že 45 dní léčby OAC může nahradit duální antiagregační terapii (100 mg/den kyselina acetylsalicylová a 75 mg/den klopidogrel).14 V současné době většina Center doporučuje duální antiagregáty po dobu 1 až 3 měsíců a neurčitou antiagregační monoterapii., Trombóza zařízení je častou komplikací, ale byla popsána jak v zařízeních Watchman™, tak v zařízeních ACP. Ačkoli tato komplikace je u většiny pacientů vyřešena 2 týdny antikoagulační terapie, potenciální riziko embolie v důsledku migrace trombů z něj činí jednu z nejobávanějších komplikací., V španělština série bylo oznámeno, alarmující rychlost zařízení trombózy byla pozorována u 14% pacientů, v kontrastu s 15 Tento rozdíl v procentech trombózy může být kvůli rozdílu v citlivosti detekce: ve španělské registru, TEE navazující protokol byl mnohem delší (24 h a 1, 3, 6 a 12 měsíců) než ve většině center studoval, kde TEE byla použita pro 3 k 6 měsíců.,15 Vzhledem k tomu, že většina případů trombózy došlo u =3 měsíců a všechny byly vyřešeny podáním natrium heparin či enoxaparin po dobu 2 týdnů, určení proveditelnosti 3 měsíce antikoagulační terapie nebo více vyčerpávající follow-up by mohl být budoucí možnost, jakmile pravda výskyt zařízení trombózy byla vyjasněna. V každém případě, multidisciplinární, individuální posouzení je nutné u pacientů tohoto typu, která někdy představují tak vysoké riziko krvácení, že dokonce i krátké období antikoagulační terapie může být kontraindikováno.,
ZÁVĚRY A VYHLÍDKY PRO BUDOUCNOST
I když NVAF je již jedním z nejčastějších onemocnění v naší společnosti, její prevalence je bude v příští letech růst v důsledku postupného stárnutí populace. Z různých důvodů je neužívá 30% až 50% pacientů indikovaných pro OAC. Dnes je Laa okluze alternativou pro pacienty s nvaf a kontraindikacemi pro antikoagulační terapii., Laa okluze je efektivní a bezpečný postup, ale vyžaduje tým se zkušenostmi se strukturální intervenční kardiologií a je spojen s podstatnou křivkou učení pro operátora.
v budoucnu by mohla být Laa okluze alternativou k léčbě OAC u všech pacientů s NVAF. I když PROTECT AF studie již prokázaly, že účinnost okluze LAA je ne méně než antikoagulační terapie, počáteční křivka učení podmíněné vysokou periprocedural komplikací., Dvě nové randomizované studie-Preview a ACP-budou specificky porovnávat Laa okluzi s léčbou OAC u pacientů s NVAF, jakmile bude překonána počáteční křivka učení. Studie preview porovnává zařízení Watchman™ s warfarinem a ACP porovnává zařízení ACP s warfarinem a dabigatranem. Pokud se výsledky obou studií ukazují, že okluze LAA je ne méně úspěšný než antikoagulační terapie u pacientů s NVAF, použití postupu by mohla být rozšířena a může se stát alternativou k antikoagulační terapie u pacientů s nižším rizikovým profilem.,
střet zájmů
Xavier Freixa je proctor of St. Jude Medical.