V chemii, enantiomeru (/ɪˈnæntiəmər, ɛ-, -tioʊ-/ ə-NAN-tee-ə-mər; z řeckého ἐνάντιος (enántios) ‚naproti‘, a μέρος (méros) „část“) (také jmenoval optický izomer, antipodu, nebo optický antipod) je jedním ze dvou stereoizomerů, které jsou zrcadlové obrazy jeden druhého, že jsou non-překrývaly (ne identické), mnohem jako levé a pravé ruce jsou zrcadlové obrazy jeden druhého, že se nemůže objevit totožné jednoduše tím, že přeorientování., Jeden chirální atom nebo podobný strukturální rys ve sloučenině způsobuje, že sloučenina má dvě možné struktury, které nejsou superposable, každý zrcadlový obraz druhého. Každý člen páru se nazývá enantiomorph (enantio = opak; morph = forma); strukturální vlastnost se nazývá enantiomerismus. Přítomnost více chirálních rysů v dané sloučenině zvyšuje počet možných geometrických forem, i když stále mohou existovat dvojice dokonalých zrcadel.,
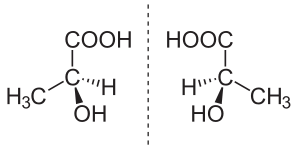
vzorek chemické látky je považován za enantiopur (také nazývaný enantiomericky čistý), pokud má v mezích detekce molekuly pouze jedné chirality.,
, Když se objeví v symetrické prostředí, enantiomery mají stejné chemické a fyzikální vlastnosti, s výjimkou jejich schopnost otáčet rovinu polarizovaného světla (+/−) o stejnou částku, ale v opačných směrech (i když polarizované světlo lze považovat za asymetrickou střední). Tyto sloučeniny jsou proto popsány jako opticky aktivní, s termíny specifické pro každý enantiomer na základě směru: pravotočivý sloučenina otáčí světlo ve směru hodinových ručiček (+) směru vzhledem k tomu, že levotočivý sloučenina otáčí světlo v proti směru hodinových ručiček (–) směru., Směs stejného počtu obou enantiomerů se nazývá racemická směs nebo racemát. V racemická směs, množství pozitivní rotace je přesně vyváženo tím, že na stejné množství negativní rotace, takže čistý rotace je nulová (směs není opticky aktivní). Pro všechny záměry a účely mají páry enantiomerů stejnou Gibbsovu volnou energii., Nicméně, teoretická fyzika předpovídá, že v důsledku porušení parity slabé jaderné síly (jedinou silou v přírodě, které mohou „říct, levou od pravé“), tam je vlastně za minutu rozdíl v energii mezi enantiomery (v řádu 10-12 eV nebo 10-10 kJ/mol nebo méně) kvůli slabé neutrální stávající mechanismus. Tento rozdíl v energii je mnohem menší než energetické změny způsobené i triviální změnou molekulární konformace a příliš malé na měření současnou technologií, a proto je chemicky bezvýznamný.,
členové enantiomeru mají často různé chemické reakce s jinými enantiomerovými látkami. Protože mnoho biologických molekul je enantiomerů, někdy existuje výrazný rozdíl v účincích dvou enantiomerů na biologické organismy. Například u léků je často za požadované fyziologické účinky zodpovědný pouze jeden z enantiomerů léku, zatímco druhý enantiomer je méně aktivní, neaktivní nebo někdy dokonce produktivní z nežádoucích účinků., Díky tomuto objevu mohou být vyvinuty léky složené pouze z jednoho enantiomeru („enantiopure“), aby lék fungoval lépe a někdy eliminoval některé vedlejší účinky. Příkladem je eszopiclone (Lunesta), což je jen jediný enantiomer staršího racemického léčiva zvaného zopiclon. Jeden enantiomer je zodpovědný za všechny požadované účinky, zatímco druhý enantiomer se zdá být neaktivní, takže dávka eszopiclone je, že polovina z zopiclone.
V chemické syntéze enantiomerů látek, non-enantiomerů prekurzory nevyhnutelně produkují racemickou směsí., Při absenci účinné enantiomerní prostředí (předchůdce, chirální katalyzátor, nebo kinetické rozlišení), oddělení racemická směs do jeho enantiomerní složek je nemožné, i když některé racemickou směsí spontánně krystalizovat ve formě racemický konglomerát, ve kterém krystaly z enantiomerů jsou fyzicky odděleny a mohou být odděleny mechanicky (např. enantiomery kyseliny vinné, jejíž průzračné enantiomery byly odděleny pinzetou tím, Pasteur)., Většina racemátů však krystalizuje v krystalech obsahujících oba enantiomery v poměru 1: 1 uspořádaném v pravidelné mřížce.