Vzdělávací Cíle
- Znát fyzikální vlastnosti iontových a molekulárních látek.
fyzický stav a vlastnosti určité látky závisí z velké části na typu chemických vazeb, zobrazí se., Molekulární sloučeniny, někdy se nazývá 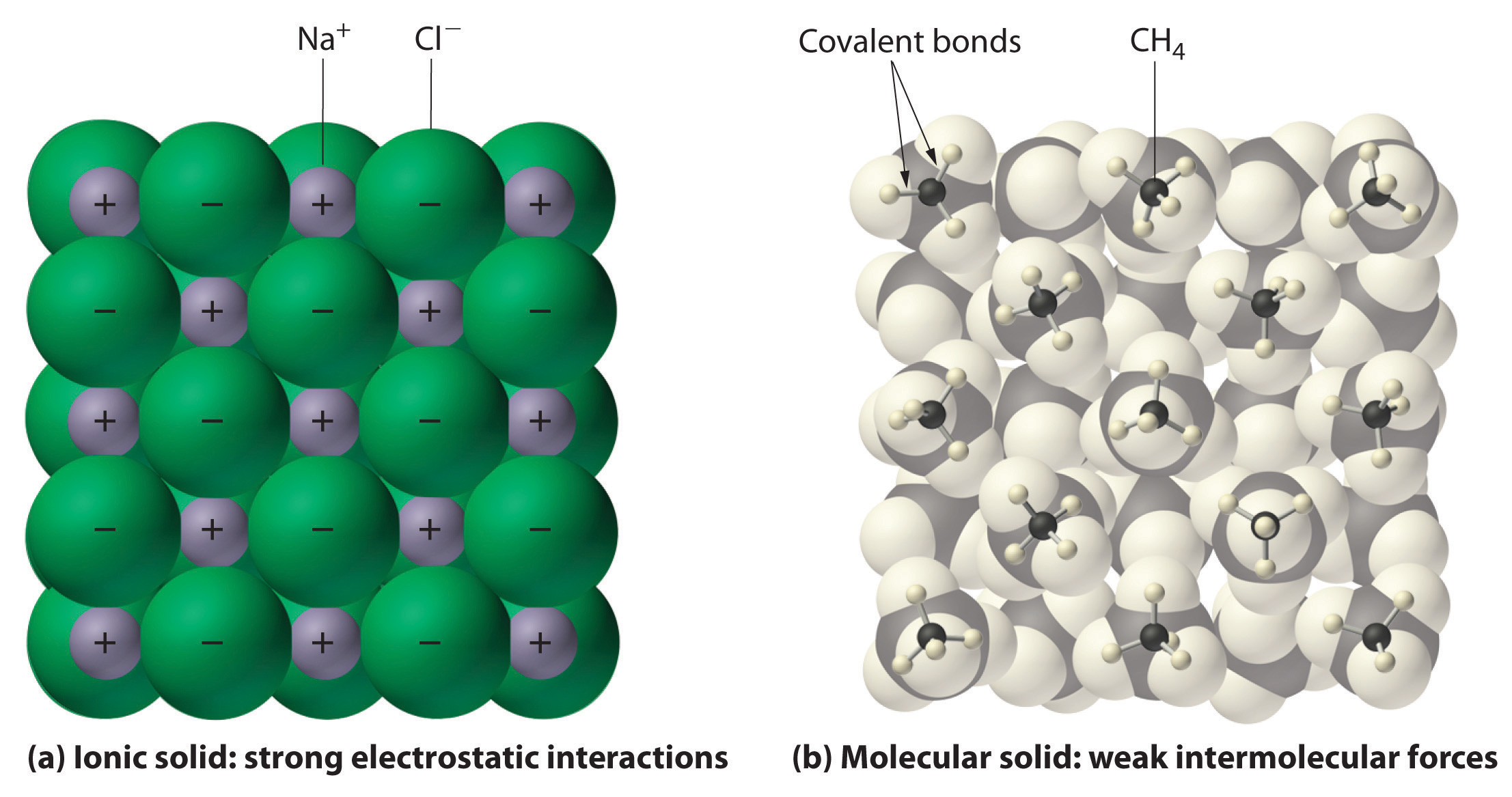 kovalentní sloučeniny, zobrazení širokou škálu fyzikálních vlastností v důsledku různých typů mezimolekulárních atrakcí, jako jsou různé druhy polární interakce. Body tání a varu molekulárních sloučenin jsou obecně poměrně nízké ve srovnání s body iontových sloučenin. Je to proto, že energie potřebná k naruší mezimolekulární síly mezi molekulami je mnohem méně, než energie potřebná k přerušení iontové vazby v krystalické iontové sloučeniny (Obrázek \(\PageIndex{1}\)) ., Iontové pevné látky se obvykle taví při vysokých teplotách a vaří se při ještě vyšších teplotách. Například, chlorid sodný taje při 801 °C a vaří při 1413 °C. (pro srovnání, molekulární sloučenina voda taje při 0 °C a vře při 100 °C.). Rozpustnost molekulárních sloučenin ve vodě je variabilní a závisí především na typu intermolekulárních sil.
kovalentní sloučeniny, zobrazení širokou škálu fyzikálních vlastností v důsledku různých typů mezimolekulárních atrakcí, jako jsou různé druhy polární interakce. Body tání a varu molekulárních sloučenin jsou obecně poměrně nízké ve srovnání s body iontových sloučenin. Je to proto, že energie potřebná k naruší mezimolekulární síly mezi molekulami je mnohem méně, než energie potřebná k přerušení iontové vazby v krystalické iontové sloučeniny (Obrázek \(\PageIndex{1}\)) ., Iontové pevné látky se obvykle taví při vysokých teplotách a vaří se při ještě vyšších teplotách. Například, chlorid sodný taje při 801 °C a vaří při 1413 °C. (pro srovnání, molekulární sloučenina voda taje při 0 °C a vře při 100 °C.). Rozpustnost molekulárních sloučenin ve vodě je variabilní a závisí především na typu intermolekulárních sil.
obrázek \(\PageIndex{1}\) interakce v iontových a kovalentních pevných látkách.,
(a) kladně a záporně nabité ionty v iontové pevné jako
chlorid sodný (NaCl) jsou drženy pohromadě pomocí silné elektrostatické interakce.
(b) V tomto zastoupení balení metanu (CH4) molekul v pevné methanu,
typický molekulární pevné látky, metan molekuly jsou drženy pohromadě
v pevné pouze relativně slabé mezimolekulové síly, i když
atomy v každé metanu molekuly jsou drženy pohromadě pomocí silné kovalentní vazby.,
protože molekulární sloučeniny jsou složeny z neutrálních molekul, jejich elektrická vodivost je obecně poměrně špatná, ať už v pevném nebo kapalném stavu. V pevné formě není iontová sloučenina elektricky vodivá, protože její ionty nejsou schopny proudit („elektřina“ je tok nabitých částic). Při roztavení však může vést elektřinu, protože její ionty se mohou volně pohybovat kapalinou (obrázek \(\PageIndex{2}\); Video \(\PageIndex{1}\)).,

Obrázek \(\PageIndex{2}\) chlorid Sodný taje při 801 °C a vede elektřinu, když je roztavený. (credit: změna práce Marka Blaser a Matt Evans)
Vodivosti Roztavené Soli
Video \(\PageIndex{1}\) podívejte se na toto video vidět, směs soli rozpustit a vedení elektřiny.
níže uvedená tabulka shrnuje některé rozdíly mezi iontovými a molekulárními sloučeninami.,>
rozpustnost ve Vodě
Jeden typ molekulární sloučenina chová zcela jinak, než je popsáno tak daleko., Kovalentní síťová pevná látka je sloučenina, ve které jsou všechny atomy navzájem spojeny kovalentními vazbami. Diamant se skládá výhradně z atomů uhlíku, z nichž každý je spojen se čtyřmi dalšími atomy uhlíku v čtyřstěnné geometrii. Tavení kovalentní pevné sítě není dosaženo překonáním relativně slabých intermolekulárních sil. Spíše musí být všechny kovalentní vazby přerušeny, což je proces, který vyžaduje extrémně vysoké teploty. Diamant se ve skutečnosti vůbec neroztaví. Místo toho se odpařuje na plyn při teplotách nad \(3500^\text{o} \ text{C}\).,
Shrnutí
- fyzikální vlastnosti materiálu jsou ovlivněny mezimolekulárních sil drží molekuly pohromadě.
- iontové sloučeniny obvykle tvoří tvrdé krystalické pevné látky s vysokými teplotami tání. Kovalentní molekulární sloučeniny se naproti tomu skládají z diskrétních molekul držených pohromadě slabými intermolekulárními silami a mohou to být plyny, kapaliny nebo pevné látky při pokojové teplotě a tlaku.
- iontové sloučeniny v roztavené formě nebo v roztoku mohou vést elektřinu, zatímco molekulární sloučeniny ne..,
Přispěvatelé
-
Marisa Alviar-Agnew (Sacramento City College)
-
Paul Flowers (University of North Carolina – Pembroke), Klaus Theopold (University of Delaware) a Richard Langley (Stephen F. Austin State University) s přispívajících autorů. Obsah učebnice produkovaný OpenStax College je licencován pod licencí Creative Commons Attribution License 4.0. Stáhněte si zdarma na http://cnx.org/contents/85abf193-2bd…[email protected]).,
-
CK-12 Foundation Sharon Bewick, Richard Parsons, Therese Forsythe, Shonna Robinson, a Jean Dupon.