Nonvalvular fibrilație atrială (NVAF) este cea mai frecventă aritmie în Spania. Incidența este strâns legată de vârstă, cu prevalență apropiată de 25% la pacienții cu vârsta peste 80 de ani.1 Printre multe procese asociate cu NVAF, accident vascular cerebral de cardioembolic origine este, probabil, cea mai gravă complicație deoarece duce la rate ridicate de invaliditate și mortalitate.,2 O altă problemă asociată cu fibrilația atrială este necesitatea terapiei anticoagulante orale (OAC) pentru a preveni evenimentele cardioembolice. Această nevoie crește odată cu vârsta înaintată, deoarece riscul unui eveniment este și mai mare.1 mai mult, riscul de complicații asociate cu terapia anticoagulantă, în special a sângerării, crește, de asemenea, la acești pacienți.3 în prezent, ocluzia percutanată a apendicelui atrial stâng (LAA) este o alternativă pentru pacienții cu FANV și contraindicații la tratamentul cu OAC.,4,5
terapia anticoagulantă orală: eficacitate și limitări
terapia anticoagulantă cu antagoniști ai vitaminei K este considerată tratamentul standard pentru FANV. Principalele probleme cu aceste medicamente sunt riscul crescut de sângerare, nevoia de controale periodice, interacțiunea cu alimentele sau alte medicamente și instabilitatea acțiunii medicamentului în unele cazuri. Se estimează că între 30% și 50% dintre pacienții indicați pentru OAC nu le primesc.6 odată cu introducerea de noi anticoagulante,cum ar fi dabigatran,7 apixaban,8 și rivaroxaban, 9 managementul acestor pacienți s-ar putea schimba., Oricare ar fi cazul și, în ciuda profilului lor de acțiune mai stabil și mai sigur, riscul de sângerare, cu o rată anuală cuprinsă între 2, 1% și 3, 6%, continuă să fie călcâiul principal al lui Ahile al acestor noi agenți (tabel). De fapt, registrele mai recente indică faptul că incidența evenimentelor cardioembolice și hemoragia secundară dabigatranului ar putea fi similare cu cele ale warfarinei.10 în ciuda introducerii de noi agenți anticoagulanți, procentul pacienților indicați pentru OAC, dar care nu primesc tratament, rămâne în jur de 40%.,11 în fața aderenței slabe la terapie și a riscului persistent de hemoragie, nevoia de alternative la terapia anticoagulantă a devenit o prioritate pentru acești pacienți.apendicele ATRIAL stâng: funcție, anatomie și indicații pentru ocluzie
LAA este o rămășiță embriologică, iar funcția sa principală este de a controla volumul sângelui. Acesta este situat foarte aproape de artera circumflexă stângă, care se învecinează la nivelul superior cu vena pulmonară superioară stângă și la nivelul inferior cu supapa mitrală., Morfologia LAA este extraordinar de eterogenă de la un pacient la altul și există adesea mai mult de un lob. În ritmul sinusal, LAA este o structură contractilă care își golește conținutul la fiecare bătaie a inimii. În fibrilația atrială, LAA își pierde capacitatea contractilă și se dilată, ducând la o încetinire a fluxului sanguin, cu riscul crescut de tromboză. În studiile de patologie ale pacienților cu NVAF, 91% din trombi localizați în atriul stâng se găsesc în LAA., Acest lucru a condus la convingerea că ocluzia percutanată laa ar putea fi o strategie eficientă de prevenire a riscului cardioembolic la pacienții cu NVAF.ocluzia percutanată LAA este încă în stadiul inițial și trebuie să treacă câțiva ani înainte de a putea obține o imagine mai fiabilă a rolului său la pacienții cu NVAF. Chiar dacă, în viitor, ar putea constitui o alternativă reală pentru pacienții fără contraindicații pentru OAC, în prezent utilizarea sa ar trebui rezervată acelor pacienți cu contraindicații la terapia anticoagulantă, așa cum se recomandă în ghidurile Europene (indicația IIb).,5 de fapt, majoritatea procedurilor la pacienții care primesc terapie anticoagulantă sunt menționate fie de serviciul de Neurologie după un episod de sângerare intracraniană, fie de Gastroenterologie după observarea sângerării digestive recurente fără o cauză tratabilă. Lipsa alternativelor valide la OAC pentru a preveni riscul cardioembolic, care este în general ridicat, deoarece aceștia sunt de obicei pacienți mai în vârstă cu multiple patologii, fac ocluzia LAA o opțiune extrem de atractivă pentru acești pacienți., Raportul normalizat internațional labil sau apariția unui eveniment cardioembolic în ciuda tratamentului cu OAC și a raportului normalizat internațional adecvat sunt alte contexte în care ocluzia percutanată laa ar putea fi justificată. În orice caz, multidisciplinare, individualizat decizii sunt necesare pentru a evalua atât cardioembolic și riscul de sângerare și alte esențiale de factori cum ar fi eficacitatea tratamentului, fragilitatea pacientului, sau aderența la tratament, mai ales cu OAC.dispozitivul PLAATO™ a fost primul ocluzor percutanat laa(Fig. 1)., În ciuda rezultatelor preliminare bune în ceea ce privește eficacitatea și siguranța, programul de dezvoltare a fost suspendat și dispozitivul a dispărut de pe piață.în prezent ,cele două dispozitive utilizate cel mai frecvent la nivel mondial sunt sistemul Watchman™ (Boston Scientific; Boston, Massachusetts, Statele Unite) și mufa cardiacă Amplatzer™ (ACP) (St.Jude Medical; Minneapolis, Minnesota, Statele Unite) (Fig. 1). La fel ca sistemul PLAATO™, ambele sunt implantate pe cale transseptală folosind accesul la vena femurală., Ambele proteze sunt foarte flexibile și au un sistem de fire de ghidare stabilizatoare care se ancorează la peretele LAA și astfel evită embolizarea. Diferența principală dintre cele două dispozitive este însă în forma lor. Paznicul™ sistem este implantat la 10 mm de la LAA ostium, și, prin urmare, nu-l acopere; ACP conține un lob, care este implantat 10-15 mm de la ostium și un disc care acoperă complet LAA ostium (Fig. 2). Un ACP de a doua generație numit Amplatzer™ Amulet™ a apărut recent pe piață. Dispozitivul Amulet™ (Fig ., 1) este, de asemenea, în formă de lob și are un disc ca ACP, dar are modificări care facilitează pregătirea și implantarea dispozitivului și, în același timp, minimizează riscul de embolizare și tromboză.
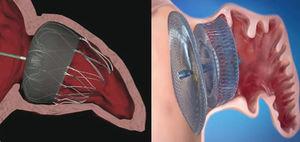
poziția dispozitivelor de conectare cardiacă Watchman™ și Amplatzer™ după implantare în apendicele atrial stâng., Paznicul™ dispozitiv implantat la 10 mm de la ostium din apendicele atrial stâng (stânga) și Amplatzer™ Cardiace Conectați dispozitivul cu lobul implantat la 10 mm de la ostium și discul care acoperă intrarea în apendicele atrial stâng (dreapta).
Numeroase registre atesta eficacitatea și siguranța Paznicul™ sistem și ACP, dar ambele necesita un nu-neglijabil implantare curbă de învățare., A PROTEJA AF studiu,12 singurul studiu randomizat care să compare warfarina cu LAA ocluzie (Paznic™) la pacienții cu NVAF, a arătat că LAA ocluzie este nu mai puțin succes decât warfarina ceea ce privește obiectivul principal (combinate accident vascular cerebral, embolie sistemică, și cardiovasculare sau de deces inexplicabil), dar a arătat o îngrijorătoare rata de periprocedural evenimente, cu 4.4% incidența severe revărsat pericardic., Această problemă inițială a fost atribuită curbei de învățare a operatorului: cu experiența operatorului, rata complicațiilor a scăzut, iar procentul de implantări reușite s-a îmbunătățit semnificativ. În prezent (pentru ambele dispozitive) mai mult de 95% din implantări sunt în general reușite, iar rata de efuziune pericardică severă este
considerații tehnice
tehnica percutanată de ocluzie laa necesită o echipă cu experiență în boala congenitală/structurală., Deși unele grupuri utilizează numai ecocardiografie intracardiacă sau chiar control angiografic pentru a ghida procedura și pentru a evita intubarea pacientului, majoritatea centrelor utilizează ecocardiografie transesofagiană (TEE) sub anestezie generală. Din punct de vedere structural, LAA are pereți foarte fini și o morfologie eterogenă care poate ascunde microtrombozele din TEE. Experiența operatorului este esențială pentru a minimiza manipularea în cadrul LAA și, astfel, pentru a reduce riscul de perforare și embolie periprocedurală., Doi dintre cei mai importanți factori care reduc la minimum manipularea în LAA sunt următoarele: a) un nivel scăzut posterior transseptal puncție, care facilitează o abordare frontală a LAA, și b) un studiu detaliat al LAA, dacă este posibil, cu TEE și angiografie, în scopul de a stabili LAA morfologie și de a obține exacte măsuri care să faciliteze selectarea occluder dimensiune. Se recomandă efectuarea măsurătorilor la volumul normal al sângelui, deoarece dimensiunea LAA poate varia semnificativ în funcție de nivelul de hidratare al pacientului., În timpul procedurii, pacienții au tendința de a deveni deshidratat; prin urmare, este recomandat ca atriul stâng presiune se determină și lichide administrate pentru a menține >10 mmHg a presiunii înainte de a lua măsurători.aceasta este o procedură relativ nouă și, chiar dacă TEE este standardul imagistic, modul imagistic ideal rămâne necunoscut. Morfologia LAA este ovală la 80% dintre pacienți, astfel încât diametrele variază de obicei din cauza axelor scurte și lungi. Această diferență poate trece neobservată cu tehnici imagistice 2-dimensionale., Ca și în procedurile precum înlocuirea percutanată a valvei aortice, TEE 3-dimensională sau tomografia cardiacă pot furniza informații spațiale care pot ajuta la optimizarea strategiei de implantare și la selectarea mărimii dispozitivului.semnificația scurgerilor periprostetice în timpul urmăririi rămâne incertă. O SUBANALIZĂ de studiu Af PROTECT nu a găsit nicio relație între scurgeri și apariția evenimentelor clinice., În schimb, în studiile privind rezultatele chirurgiei coronariene cardiace, excizia incompletă A LAA la pacienții care au avut ocluzie profilactică chirurgicală laa a fost asociată cu o rată mai mare de evenimente cardioembolice. În timp ce așteptăm să devină disponibile noi studii care pot sau nu să confirme această relație, ar trebui să încercăm să prevenim scurgerile periprostetice. Prin urmare, se recomandă ca dispozitivul să fie ceva mai mare decât ar sugera TEE și măsurile angiografice, deoarece acest lucru face posibilă reducerea ratei scurgerilor reziduale fără a crește riscul ruperii peretelui LAA.,13
recomandările antitrombotice Postprocedurale sunt o altă problemă controversată. În studiul PROTECT AF, OAC a fost administrat timp de 45 de zile postimplantare și suspendat dacă TEE a prezentat o ocluzie LAA adecvată.12 recent, studiul ASAP a arătat că 45 de zile de tratament cu OAC pot înlocui terapia dublă antiplachetară (100 mg/zi acid acetilsalicilic și 75 mg/zi clopidogrel).14 în prezent, majoritatea centrelor recomandă antiplachetare duale timp de 1 până la 3 luni și monoterapie antiplachetară nedeterminată., Tromboza dispozitivului este o complicație rară, dar a fost descrisă atât în dispozitivele Watchman™, cât și în dispozitivele ACP. Deși această complicație este rezolvată prin 2 săptămâni de terapie anticoagulantă la majoritatea pacienților, riscul potențial de embolie datorat migrației trombilor îl face una dintre cele mai temute complicații., În numai o serie spaniol a raportat, un ritm alarmant de dispozitiv tromboză a fost observată la 14% dintre pacienți, în contrast cu 15 Această diferență în procent de tromboză ar putea fi din cauza la o schimbare în sensibilitate de detectare: în spaniolă registry, TEE follow-up protocol a fost mult mai mult timp (24 h și 1, 3, 6 și 12 luni) decât în cele mai multe centre de studiat, unde TEE a fost folosit timp de 3 până la 6 luni.,15 având în vedere că majoritatea cazurilor de tromboză au apărut la 3 luni și toate au fost rezolvate prin administrarea heparinei de sodiu sau a enoxaparinei timp de 2 săptămâni, determinarea fezabilității a 3 luni de tratament anticoagulant sau urmărirea mai exhaustivă ar putea fi o opțiune viitoare, odată ce incidența reală a trombozei dispozitivului a fost clarificată. În orice caz, este necesară o evaluare multidisciplinară și individualizată la pacienții de acest tip, care prezintă uneori un risc atât de mare de sângerare încât chiar și perioadele scurte de terapie anticoagulantă ar putea fi contraindicate.,chiar dacă NVAF este deja una dintre cele mai frecvente boli din societatea noastră, prevalența acesteia va crește în următorii ani datorită îmbătrânirii progresive a populației. Din diferite motive, între 30% și 50% dintre pacienții indicați pentru OAC nu le iau. Astăzi, ocluzia LAA constituie o alternativă pentru pacienții cu FANV și contraindicații pentru terapia anticoagulantă., Ocluzia LAA este o procedură eficientă și sigură, dar necesită o echipă cu experiență în cardiologia intervențională structurală și este asociată cu o curbă de învățare substanțială pentru operator.în viitor, ocluzia LAA ar putea fi o alternativă la tratamentul cu OAC pentru toți pacienții cu FANV. Deși studiul PROTECT AF a dovedit deja că eficacitatea ocluziei LAA nu este mai mică decât cea a terapiei anticoagulante, curba inițială de învățare a condiționat o rată ridicată de complicații periprocedurale., Două noi studii randomizate-prevalează și ACP-vor compara în mod specific ocluzia LAA cu tratamentul OAC la pacienții cu NVAF odată ce curba inițială de învățare a procedurii a fost depășită. Studiul PREVAIL compară dispozitivul Watchman™ cu warfarina, iar ACP compară dispozitivul ACP cu warfarina și dabigatranul. Dacă rezultatele celor două studii arată că LAA ocluzie este nu mai puțin succes decât terapia anticoagulantă la pacienții cu NVAF, utilizarea de procedura ar putea fi extinse și ar putea deveni o alternativă la terapia anticoagulantă la pacienții cu un profil de risc mai scăzut.,Xavier Freixa este proctor al Sf.