oțelul este cel mai obișnuit material utilizat astăzi. Cu toate acestea, oțelul are un dezavantaj mare – rata ridicată de coroziune. Protecția structurilor și componentelor metalice are, prin urmare, o mare importanță economică.cea mai bună protecție împotriva coroziunii pentru oțel este obținută cu zinc. Acoperirile cu Zinc pe oțel protejează împotriva coroziunii în două moduri:
- printr-un efect de barieră, adică împiedică oxigenul și umiditatea să ajungă la suprafața oțelului.,
- oferind protecție catodică la zgârieturi, așchii, margini etc.
zincul este un metal cu un potențial galvanic relativ scăzut și o tendință ridicată de corodare. Cu toate acestea, rata de coroziune este scăzută în majoritatea mediilor, deoarece suprafața acoperirii este acoperită rapid cu produse de coroziune, care protejează ulterior împotriva coroziunii ulterioare. când un obiect galvanizat la cald părăsește baia de zinc, suprafața obiectului este imediat atacată de oxigen în aer., Stratul de oxid rezultat are o capacitate foarte mică de a proteja împotriva coroziunii. Cu toate acestea, apa și dioxidul de carbon din aer schimbă rapid stratul de oxid în carbonații de zinc. Acestea dau un strat sigilat cu o aderență foarte bună. Deoarece carbonații au o solubilitate foarte scăzută în apă, aceștia oferă o protecție excelentă suprafeței stratului de zinc. Suprafața originală lucioasă cu un luciu metalic dispare pentru a fi înlocuită cu o culoare mată, gri deschis (fig.1).

Fig 1., Suprafața expusă a unui strat de zinc cu strat exterior de zinc pur. Suprafața lucioasă dispare pentru a fi înlocuită cu produse de coroziune gri (uneori numite patină de zinc).

Fig. 2. Suprafață decolorată pe coloana de iluminat. Acoperirea constă în principal dintr-un aliaj de fier-zinc care se extinde la suprafață. Fierul este expus în timpul coroziunii, ceea ce duce la formarea ruginii. Este doar rugina de suprafață și are doar o semnificație estetică.,aerul exterior conține o cantitate mai mare sau mai mică de elemente corozive — gaze, funingine, umiditate (ceață, rouă, ploaie, zăpadă), praf inert și agresiv. Nivelurile pot varia în funcție de locație și de timpul anului. Sulfații și sulfiții de zinc sunt solubili în apă și au o aderență slabă la suprafața zincului. Prin urmare, acestea sunt spălate cu ușurință de ploaie. O suprafață proaspătă de zinc este apoi expusă atacului oxigenului din aer și se repetă ciclul de coroziune. Prin urmare, coroziunea în aerul care conține oxizi de sulf este mai mare decât în aerul curat., Cu toate acestea, cantitatea de dioxid de sulf din atmosferă a scăzut drastic în ultimii ani și, prin urmare, coroziunea zincului a scăzut și ea.în mediile marine, coroziunea zincului este influențată de conținutul de sare al aerului. Cu toate acestea, aerul marin conține cantități mici de săruri de magneziu, cu influențe bune de pasivare. Prin urmare, coroziunea nu este la fel de mare cum ar fi de așteptat. Conținutul de sare al aerului se reduce rapid departe de coastă.coroziunea zincului este influențată de mulți factori., Aceasta înseamnă că nu poate fi dată o formulă general aplicabilă pentru ratele de coroziune. Acoperirile cu Zinc au fost totuși utilizate mult timp, într-o gamă largă de condiții, pentru a proteja oțelul de rugină. De asemenea, au fost efectuate un număr mare de teste pe termen lung. Cunoștințele despre coroziunea zincului și ratele de coroziune în diferite medii sunt, prin urmare, bune. Astăzi, există exemple de acoperiri de zinc care au fost expuse de mai bine de o sută de ani.culoarea produselor de coroziune variază în funcție de mediul în care sunt formate., Mediile Marine oferă produse de coroziune oarecum mai albe în comparație cu mediile rurale și urbane. Produsele de coroziune sunt de obicei cele mai întunecate în mediile urbane.
coroziunea în lichide
suprafața zincului este în general acoperită cu un strat protector de produse de coroziune atunci când este scufundată într-un lichid. Cu toate acestea, lichidele pot fi acide sau alcaline și pot conține particule dizolvate sau solide de substanțe agresive. Temperatura și debitul lichidului sunt, de asemenea, semnificative., Toate acestea înseamnă că stratul protector poate avea o compoziție foarte variată sau poate să nu se formeze deloc.coroziunea Electro-chimică, care joacă un rol subordonat în aer, are o importanță mai mare în lichide. Gradul de coroziune electro-chimică depinde de conductivitatea electrică a lichidului, care afectează influența protectoare a stratului de zinc pe suprafețe mai mari sau mai mici.valoarea pH-ului lichidului este de cea mai mare importanță. Rata de coroziune a zincului este în mod normal scăzută și stabilă în intervalul de pH 5,5-12,5, la temperaturi cuprinse între 0 și 20 °C., Coroziunea în afara acestui interval este de obicei mai rapidă.apa tare, care conține var și magneziu, este mai puțin agresivă decât apa moale. Împreună cu dioxidul de carbon, aceste substanțe formează carbonați puțin solubili pe suprafața zincului, protejând zincul împotriva coroziunii ulterioare.apa moale atacă adesea zincul, deoarece absența sărurilor înseamnă că stratul protector nu poate fi format. apele moi agresive pot fi găsite în multe râuri și lacuri din Finlanda, Norvegia, Suedia și medii similare.
dacă debitul este mai mare de 0.,5 m/s formarea stratului protector pe suprafața zincului este inhibată și coroziunea accelerează.
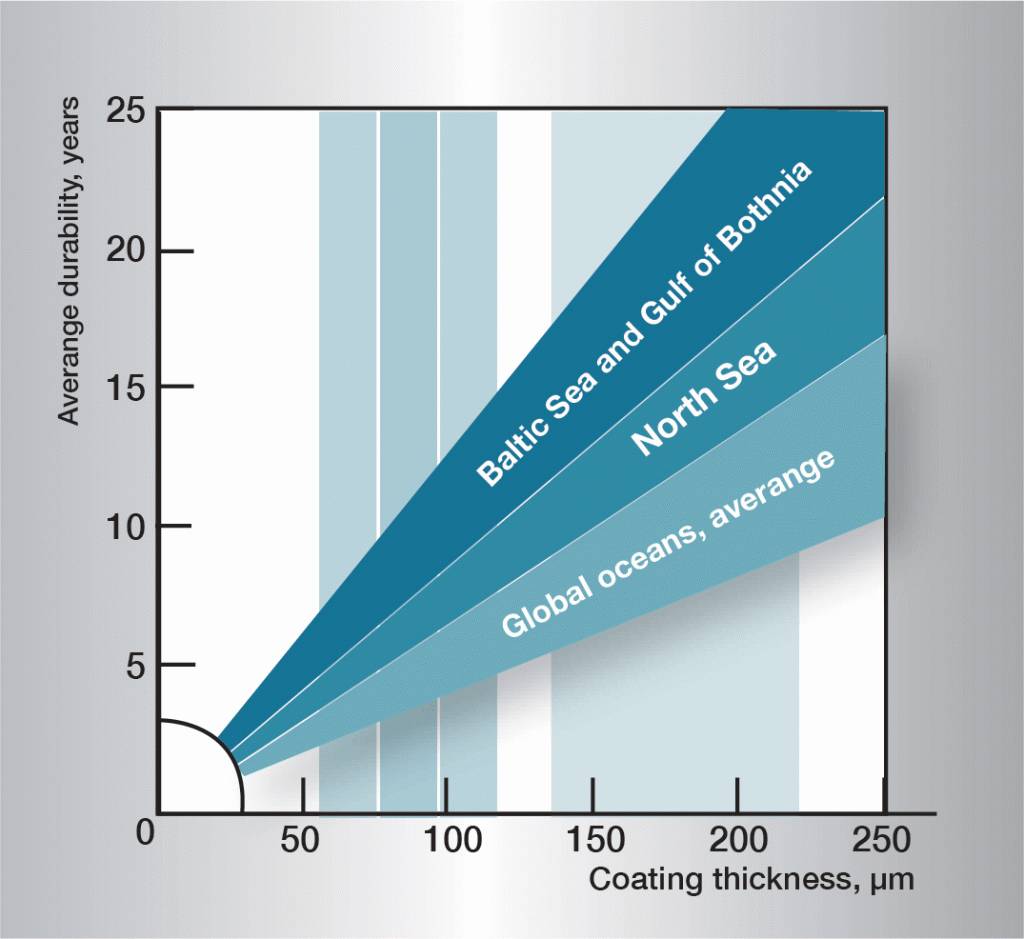
temperatura apei este de mare importanță pentru rata de coroziune. Peste aproximativ 55 °C, produsele de coroziune care formează straturi dobândesc o structură cu granulație grosieră și pierd aderența la suprafața zincului. Acestea sunt ușor dislocate și expun zinc nou, proaspăt pentru un atac continuu și rapid de coroziune. Rata de coroziune atinge un maxim la aproximativ 70 °C, după care scade astfel încât la 100 °C să fie aproximativ aceeași ca la 50 °C.,secvența de coroziune în apă este foarte complexă și este influențată în mare măsură de variații foarte mici în compoziția apei. Prin urmare, este dificil să se prevadă norme general aplicabile. Informațiile din Figura 3 se bazează pe experiența practică și oferă orientări pentru unele tipuri diferite de apă.
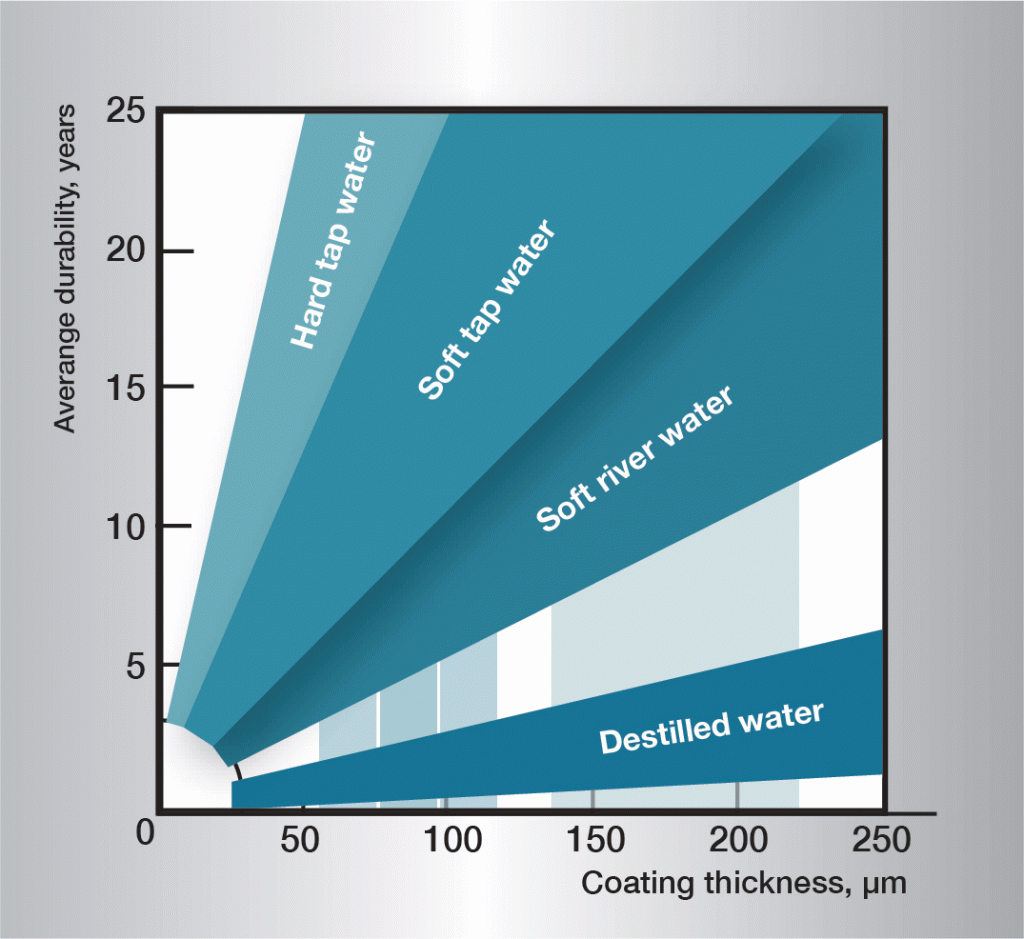
Fig. 3. Durata de viață în diferite ape.,
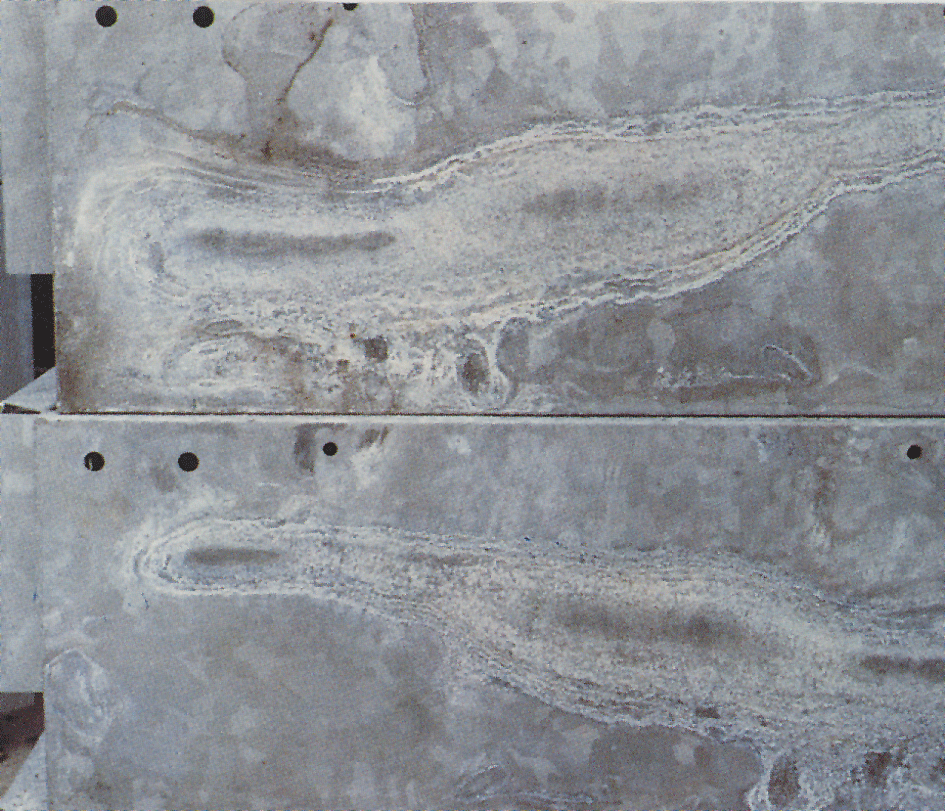
Ud-depozitare pata
Uneori, un alb, făinos și voluminos strat numit umed-depozitare pata, sau rugina albă, apare pe suprafețe galvanizate (fig.4). Rugina albă se formează pe materiale cu suprafețe noi galvanizate, lucioase și mai ales în crăpături între foi bine ambalate, fier unghiular și materiale similare. O condiție prealabilă este ca materialul să fie expus condensului sau apei de ploaie în condiții în care umiditatea nu se poate evapora rapid., Suprafețele de Zinc care au primit deja un strat normal de protecție a produselor de coroziune sunt rareori atacate. Când acoperirile cu zinc sunt expuse la aer, se formează oxid de zinc și hidroxid de zinc. Sub influența dioxidului de carbon din aer, acestea sunt transformate în carbonați de zinc bazici. Dacă accesul aerului la suprafața zincului este restricționat, ca în crăpăturile înguste, atunci zona primește dioxid de carbon insuficient pentru a permite formarea stratului normal de carbonați.
stratul de pete de depozitare umedă este voluminos și poros și este atașat doar slab la suprafața zincului., Ca urmare, protecția împotriva atacului continuu nu există. Prin urmare, coroziunea poate continua atât timp cât umiditatea rămâne pe suprafețe. Când a apărut pata de depozitare umedă, obiectul trebuie stivuit pentru a permite suprafețelor să se usuce rapid. Acest lucru va opri atacul și, cu acces liber la aer, se va forma stratul protector normal. Pata de depozitare umedă este spălată treptat, iar acoperirea capătă un aspect normal pentru oțelul galvanizat la cald expus., deoarece acest produs de coroziune albă este foarte voluminos (de aproximativ 500 de ori mai mare decât zincul din care a fost format), poate părea grav. Cu toate acestea, pata de depozitare umedă are adesea o semnificație mică sau deloc asupra duratei de viață a protecției împotriva coroziunii. Cu toate acestea, în cazul acoperirilor foarte subțiri, de exemplu pe obiecte galvanizate, un atac sever al petelor de depozitare umedă poate fi semnificativ.
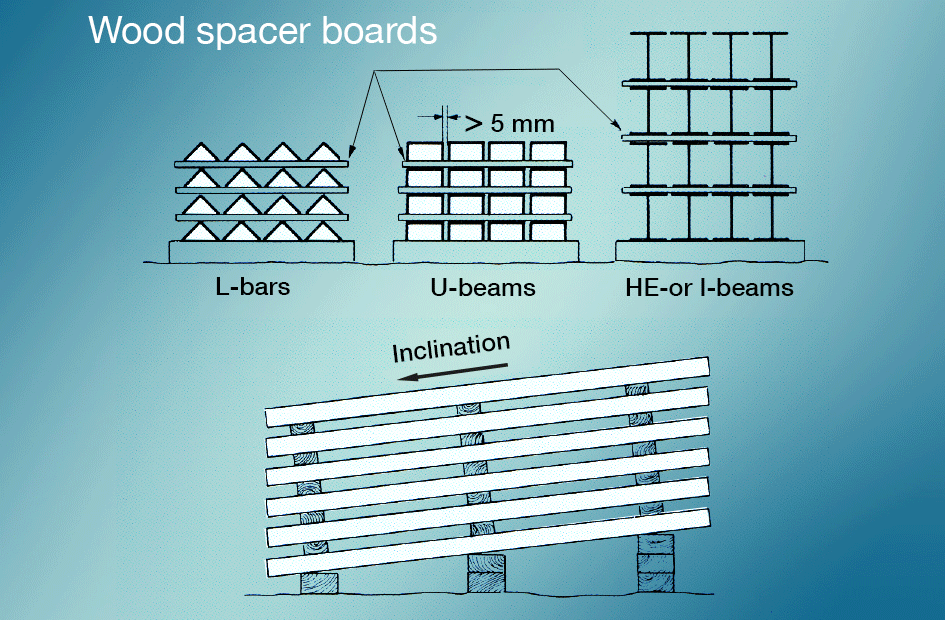
Ud-depozitare pata este cel mai bine evitate prin prevenirea recent suprafețe galvanizate la venirea în contact cu ploaie sau condens în timpul transportului., Materialele depozitate în aer liber trebuie stivuite astfel încât apa să poată curge ușor și astfel încât toate suprafețele să fie bine ventilate (fig. 5). Pictura după galvanizare oferă o protecție foarte bună. condițiile de coroziune din sol sunt foarte complicate, iar variațiile pot fi mari între diferite locații, chiar și cele aflate în imediata apropiere. Solul poate conține produse erodate, săruri libere sau legate, acizi și alcalii, amestecuri de substanțe organice, fungi oxidanți sau reducători, microorganisme etc., În funcție de structura sa, solul are grade diferite de permeabilitate la aer și umiditate. În mod normal, conținutul de oxigen este mai mic decât în aer, în timp ce conținutul de dioxid de carbon este mai mare.în general, solurile suedeze nu sunt foarte agresive. Coroziunea medie pentru zinc este de obicei luată ca 5 µm pe an. Solurile foarte agresive sunt rareori observate. În Botnia de Nord și de Vest, solurile pot conține sulf. Ele sunt adesea negre, dar se luminează atunci când sunt expuse la aer. În aceste soluri, ratele de coroziune a zincului sunt foarte mari.
O metodă de determinare a corozivității unui sol este măsurarea rezistivității acestuia., Dacă resitivitatea solului nu poate fi determinată, regulile de bază enumerate în Figura 6 pot oferi o măsură de orientare. Cu toate acestea, în ceea ce privește expunerea metalelor la sol, este recomandabil să se solicite consultanță de specialitate din surse calificate corespunzător.

coroziunii Galvanice

Dacă două metale sau aliaje, complet sau parțial înconjurat de un electrolit, sunt conectate o celulă galvanică este creat. Ce metal devine anod sau catod este determinat de potențialele lor de electrod în electrolitul în cauză. În apa de mare, care corespunde majorității condițiilor practice, unele metale și aliaje ocupă poziții diferite pe scara electrochimică, prezentată în Figura 7., dacă oțelul este conectat la cupru sau alamă, oțelul devine anodul din celulă și corodează. Cu toate acestea, dacă oțelul este conectat la cadmiu, aluminiu, zinc sau magneziu, acesta devine catod și este protejat împotriva coroziunii, în timp ce metalul anodic este consumat. Coroziunea galvanică este numită și coroziune bimetalică și este utilizată pentru a proteja structurile subacvatice de coroziune, când se numește protecție catodică.
protecția catodică oferită de acoperirile cu zinc
în oțel galvanizat la cald, zincul și oțelul sunt în contact electric bun între ele., Dacă stratul de zinc este deteriorat în prezența unui electrolit, se creează o celulă galvanică. Electrolitul poate fi condens sau apă de ploaie. Uneori întreaga structură poate fi scufundată în lichid. În această celulă, zincul devine anod sau pol de dizolvare, oțelul expus devine catod și, prin urmare, este protejat de coroziune.în faza inițială este adesea posibil să se observe o formare ust slabă pe partea expusă a suprafeței oțelului unde stratul de acoperire a fost deteriorat, dar după un timp se formează zone gri-albicioase care se răspândesc treptat pe întreaga zonă deteriorată., Acoperirea cu zinc corodează și aliajele de zinc puțin solubile coboară pe suprafața catodului, unde protejează oțelul de atacul continuu de rugină. Acest lucru este adesea numit „auto-vindecare”, care este ceva de un termen impropriu, deoarece stratul de zinc nu este, desigur, restaurat.datorită protecției catodice generate de zinc, rugina nu se poate „strecura” sub acoperire în punctul de deteriorare în modul în care se poate strecura sub filme de vopsea sau acoperiri de metale mai nobile decât oțelul., Acoperirile cu Zinc pe oțel sunt neobișnuite, deoarece o suprafață destul de mare de deteriorare a stratului de acoperire nu provoacă pierderi catastrofale de protecție împotriva ruginii. Gama de protecție catodică depinde de natura electrolitului care creează celula. Pentru structurile din atmosfere normale este obișnuit să se aștepte o acțiune de protecție pe mai mulți milimetri. Cu toate acestea, în apa de mare se pot aștepta distanțe semnificativ mai mari.
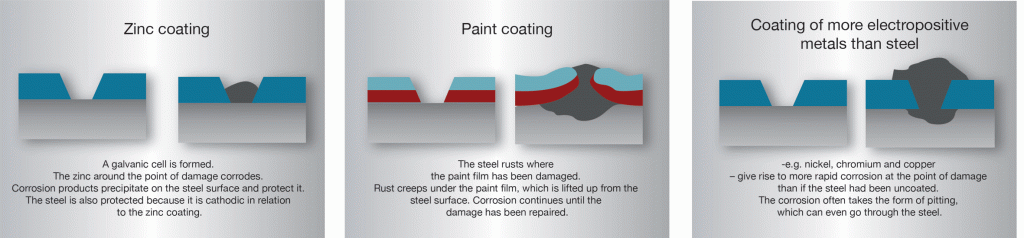
straturi de Zinc în contact cu metale neferoase
potentialul Electrochimic scară arată că zincul este mai puțin nobil decât cele mai comune metale. Aceasta înseamnă că atunci când zincul este conectat la aceste metale într-o celulă galvanică, zincul devine Polul de dizolvare. În principiu, astfel de conexiuni ar trebui evitate atunci când este posibil. O metodă bună este utilizarea unui izolator, cum ar fi plasticul sau cauciucul la îmbinare.,aluminiul și oțelul inoxidabil pot fi adesea conectate direct la Materialul galvanizat în aer sau în medii destul de uscate, fără a avea loc coroziunea vizibilă. Cu toate acestea, în apă trebuie utilizat întotdeauna un izolator.CUPRUL și aliajele de cupru sunt mai active din punct de vedere electric și există adesea o eliberare de ioni de cupru care se răspândesc pe suprafețe mari și provoacă un atac vizibil. Din acest motiv, aceste metale nu ar trebui să li se permită niciodată să intre în contact cu oțelul galvanizat și ar trebui utilizat un izolator.,
oțel galvanizat la cald în contact cu mortar, ipsos și lemn
mortar umed și zinc atac ipsos. Atacul încetează atunci când materialul se usucă. Lemnul uscat sau moderat umed, atât impregnat, cât și neimpregnat, poate fi bătut în cuie cu unghii galvanizate la cald pentru un efect bun. Cu toate acestea, în cazul unghiilor sau al uniunilor filetate care sunt expuse constant la apă, este preferat un material rezistent la acid. Alte materiale de construcție uscate, cum ar fi vata minerală, nu atacă zincul.,chiar dacă un strat galvanizat la cald este capabil să reziste la un tratament destul de dur, acesta trebuie manipulat cu grijă în timpul depozitării și transportului. În cazul mărfurilor lungi, ambalarea simplă și legarea în pachete nu numai că protejează împotriva deteriorării mecanice, dar facilitează adesea transportul în sine. Cu toate acestea, ambalarea și legarea trebuie să se facă astfel încât să se evite riscul de tulpină de depozitare umedă. Distanțierele ar trebui utilizate pentru a preveni astfel de atacuri.