Există patru legi, cunoscute ca Legile Gazelor, care descrie modul în care gazele se comporta. Cele patru legi sunt Legea lui Boyle, Legea lui Charles, Legea lui Gay-Lussac și Legea lui Avogadro.Jacques Charles, un fizician francez, a descoperit în anii 1780 că încălzirea unui gaz îl va face să se extindă cu o anumită fracțiune. Imaginea de mai jos arată cum adăugarea de căldură face ca moleculele să se miște mai repede și să lovească părțile laterale și capacul cu o forță mai mare, mișcând astfel capacul în sus pe măsură ce gazul se extinde.,
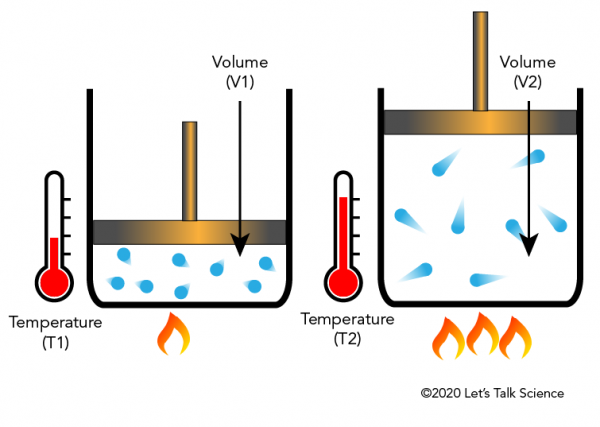
Charles de Drept în Viața de zi cu Zi
În scopul de a face un balon cu aer cald crește, căldura este adăugat la aerul din interiorul balonului. Adăugarea de căldură face ca moleculele să se deplaseze mai departe unul de celălalt.

În limbajul de zi cu zi, am putea spune că aerul din interior se extinde. Când se întâmplă acest lucru, densitatea totală (masa pe unitatea de volum) a balonului și aerul din interiorul acestuia scade. Când densitatea balonului scade pentru a fi mai mică decât densitatea aerului exterior, balonul crește. În schimb, volumul unui gaz se va micșora dacă temperatura acestuia scade. mai jos puteți vedea azotul lichid turnat peste un balon verde. Azotul lichid rece răcește aerul din interiorul balonului., Ca urmare, moleculele de aer încetinesc, determinând scăderea volumului balonului.

în Timpul sărbătorilor, cuiva poate fi folosit un curcan termometru. Un termometru de curcan este blocat în curcan în timp ce gătește și apoi apare atunci când carnea este gătită suficient. Cum funcționează această minunată tehnologie? Are legătură cu Legea lui Charles, desigur!, În interiorul termometrului de curcan este o cantitate mică de aer. Pe măsură ce temperatura crește în interiorul curcanului, aerul din interiorul termometrului de curcan se extinde. Odată ce atinge un anumit volum, vârful apare, spunându-i bucătarului că curcanul este gătit corespunzător.

Gay-Lussac Legea lui
Joseph Louis Gay-Lussac a fost un chimist francez și fizician care a descoperit în 1802 că, dacă vă păstrați volumul unui gaz constanta (cum ar fi într-un recipient închis), și se aplică de căldură, presiunea gazelor va crește. Acest lucru se datorează faptului că gazele au mai multă energie cinetică, determinându-le să lovească pereții recipientului cu mai multă forță (rezultând o presiune mai mare).
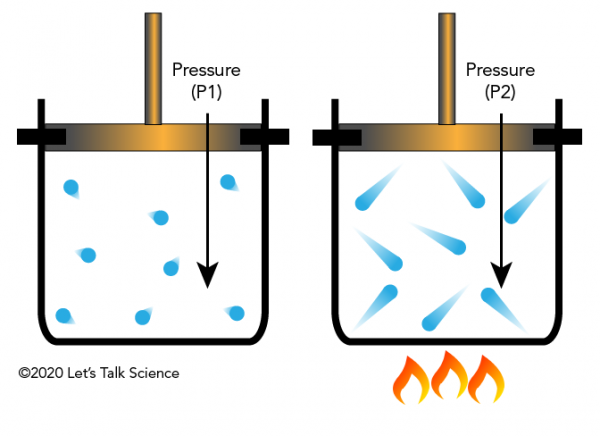
Gay-Lussac-lui în Viața de zi cu Zi
în Interiorul-o oala sub presiune de alimentare pe care doriți să gătească stă în apă. Pe măsură ce temperatura apei lichide crește, se produc vapori de apă (apă în stare gazoasă). Acești vapori nu pot scăpa de aragazul sub presiune – ceea ce înseamnă că volumul nu se schimbă. Presiunea vaporilor de apă continuă să crească până când temperatura apei și a vaporilor de apă depășesc punctul normal de fierbere al apei (100 °C). La această temperatură mai ridicată, alimentele pot fi gătite mult mai repede., Carnea dură iese, de asemenea, mult mai fragedă după ce a fost gătită într-o aragaz sub presiune.

știați că presiunea aerului din interiorul anvelopelor auto se schimbă atunci când mașina este condusă? După conducere, presiunea aerului din anvelopele unei mașini crește. Acest lucru se datorează faptului că frecarea (o forță de contact) între anvelope și drum determină încălzirea aerului din anvelope., Aerul nu se poate extinde, deoarece anvelopele sunt în esență un container cu volum fix, astfel încât presiunea crește-aceasta este legea lui Gay – Lussac!