nienowotworowe migotanie przedsionków (NVAF) jest najczęściej występującą arytmią w Hiszpanii. Częstość występowania jest ściśle związana z wiekiem, przy czym częstość występowania wynosi blisko 25% u pacjentów w wieku powyżej 80 lat.1 wśród wielu procesów związanych z NVAF, udar naczyniowo-mózgowy pochodzenia kardioembolicznego jest prawdopodobnie najpoważniejszym powikłaniem, ponieważ prowadzi do wysokiego wskaźnika niepełnosprawności i śmiertelności.,2 innym problemem związanym z migotaniem przedsionków jest potrzeba doustnej terapii przeciwzakrzepowej (oac) w celu zapobiegania zdarzeniom kardioembolicznym. Potrzeba ta rośnie wraz z zaawansowanym wiekiem, ponieważ ryzyko zdarzenia jest jeszcze większe.1 ponadto zwiększa się ryzyko powikłań związanych z leczeniem przeciwzakrzepowym, zwłaszcza krwawień, u tych pacjentów.3 obecnie okluzja przezskórnego wyrostka lewego przedsionka (LAA) jest alternatywą dla pacjentów z NVAF i przeciwwskazaniami do leczenia OAC.,4,5
doustne leczenie przeciwzakrzepowe: skuteczność i ograniczenia
leczenie przeciwzakrzepowe z antagonistami witaminy K jest uważane za standardowe leczenie NVAF. Głównymi problemami z tymi lekami są zwiększone ryzyko krwawienia, konieczność regularnych badań kontrolnych, interakcja z żywnością lub innymi lekami i niestabilność działania leku w niektórych przypadkach. Szacuje się, że nie otrzymuje ich od 30% do 50% pacjentów wskazanych do OAC.Po wprowadzeniu nowych leków przeciwzakrzepowych, takich jak dabigatran, 7 apiksaban, 8 i rywaroksaban, 9 pacjentów może ulec zmianie., Niezależnie od przypadku i pomimo bardziej stabilnego i bezpieczniejszego profilu działania, ryzyko krwawienia, którego roczna stopa wynosi od 2,1% do 3,6%, nadal jest główną piętą achillesową tych nowych leków(tabela). W rzeczywistości, nowsze rejestry wskazują, że częstość występowania zdarzeń kardioembolicznych i krwotoków wtórnych do dabigatranu może być podobna do częstości występowania warfaryny.Pomimo wprowadzenia nowych leków przeciwzakrzepowych odsetek pacjentów wskazanych do OAC, ale nieleczonych, utrzymuje się na poziomie około 40%.,11 W obliczu słabego przestrzegania terapii i utrzymującego się ryzyka krwotoku, potrzeba alternatyw dla terapii przeciwzakrzepowej stała się priorytetem dla tych pacjentów.
wyrostek przedsionkowy lewy: funkcje, anatomia i wskazania do okluzji
LAA jest pozostałością embriologiczną, a jego główną funkcją jest kontrola objętości krwi. Znajduje się bardzo blisko tętnicy lewej obwodowej, graniczącej na górnym poziomie z żyłą płucną górną lewą, a na Dolnym z zastawką mitralną., Morfologia LAA jest niezwykle niejednorodna u jednego pacjenta i często występuje więcej niż jeden płat. W rytmie zatokowym LAA jest skurczową strukturą, która opróżnia swoją zawartość przy każdym uderzeniu serca. W migotaniu przedsionków LAA traci zdolność skurczową i rozszerza się, co prowadzi do spowolnienia przepływu krwi, co w konsekwencji zwiększa ryzyko zakrzepicy. W badaniach patologicznych u pacjentów z NVAF 91% zakrzepów zlokalizowanych w lewym przedsionku znajduje się w LAA., Doprowadziło to do przekonania, że przezskórna okluzja LAA może być skuteczną strategią zapobiegania ryzyku kardioembolicznemu u pacjentów z NVAF.
przezskórna okluzja LAA jest nadal w początkowej fazie i jeszcze kilka lat musi upłynąć, zanim będziemy mogli uzyskać bardziej wiarygodny obraz jej roli u pacjentów z NVAF. Nawet jeśli w przyszłości może stanowić realną alternatywę dla pacjentów bez przeciwwskazań do stosowania OAC, obecnie jego stosowanie powinno być zarezerwowane dla pacjentów z przeciwwskazaniami do leczenia przeciwzakrzepowego, zgodnie z zaleceniami europejskimi (wskazanie IIb).,5 w rzeczywistości, większość procedur u pacjentów otrzymujących leczenie przeciwzakrzepowe są kierowane przez służby neurologii po epizodzie krwawienia wewnątrzczaszkowego, lub przez gastroenterologii po obserwacji nawracających krwawień trawiennych bez uleczalnej przyczyny. Brak ważnych alternatyw dla OAC w celu zapobiegania ryzyku kardioembolicznemu, które jest na ogół wysokie, ponieważ są to zazwyczaj starsi pacjenci z wieloma patologiami, sprawiają, że okluzja LAA jest bardzo atrakcyjną opcją dla tych pacjentów., Labile international znormalized ratio lub pojawienie się zdarzenia kardioembolicznego pomimo leczenia OAC i odpowiedniego międzynarodowego znormalizowanego ratio są innymi kontekstami, w których przezskórna okluzja LAA może być uzasadniona. W każdym razie, multidyscyplinarne, indywidualne decyzje są potrzebne do oceny zarówno cardioembolic i ryzyko krwawienia i innych istotnych czynników, takich jak skuteczność leczenia, słabość pacjenta, lub przestrzeganie leczenia, zwłaszcza z OAC.
urządzenia do okluzji lewego przedsionka
urządzenie PLAATO™ było pierwszą przezskórną okluderką LAA (rys. 1)., Pomimo dobrych wstępnych wyników pod względem skuteczności i bezpieczeństwa, program rozwojowy został zawieszony, a urządzenie zniknęło z rynku.
obecnie dwa urządzenia najczęściej używane na całym świecie to system Watchman™ (Boston Scientific; Boston, Massachusetts, Stany Zjednoczone) i wtyczka Kardiologiczna Amplatzer™ (ACP) (St.Jude Medical; Minneapolis, Minnesota, Stany Zjednoczone) (rys. 1). Podobnie jak system PLAATO™, oba są wszczepiane drogą transseptalną za pomocą dostępu żyły udowej., Obie protezy są bardzo elastyczne i posiadają system prowadnic stabilizujących, które mocują się do ściany LAA, a tym samym unikają embolizacji. Główną różnicą między tymi dwoma urządzeniami jest jednak ich kształt. System Watchman™ jest wszczepiany w odległości 10 mm od Laa ostium i dlatego go nie zakrywa; ACP zawiera płat wszczepiany w odległości 10-15 mm od ostium oraz dysk, który całkowicie zakrywa LAA ostium (rys. 2). Niedawno na rynku pojawił się ACP drugiej generacji o nazwie Amplatzer™ Amulet™. Urządzenie Amulet™ (rys., 1) ma również kształt płata i ma dysk podobny do ACP, ale posiada modyfikacje, które ułatwiają przygotowanie urządzenia i implantację, a jednocześnie minimalizują ryzyko embolizacji i zakrzepicy.
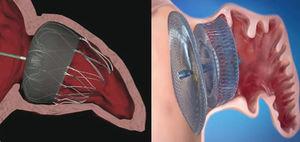
umiejscowienie wtyczek kardiologicznych Watchman™ i Amplatzer™ po wszczepieniu do lewego przedsionka., Urządzenie Watchman ™ wszczepione w odległości 10 mm od ostium lewego wyrostka przedsionkowego (po lewej) oraz urządzenie Plug-inowe Amplatzer™ z płatem wszczepionym w odległości 10 mm od ostium i krążkiem zakrywającym wejście do lewego wyrostka przedsionkowego (po prawej).
liczne rejestry potwierdzają skuteczność i bezpieczeństwo systemu Watchman™ i ACP, ale oba wymagają niezauważalnej krzywej uczenia się implantacji., Badanie PROTECT AF, 12, jedyne randomizowane badanie porównujące warfarynę z okluzją LAA (Watchman™) u pacjentów z NVAF, wykazało, że okluzja LAA jest nie mniej skuteczna niż warfaryna w odniesieniu do głównego celu (złożony Epizod naczyniowo-mózgowy, zatorowość układowa, śmierć sercowo-naczyniowa lub niewyjaśniona), ale wykazało niepokojący odsetek zdarzeń okoproceduralnych, z częstością występowania 4,4% ciężkiego wysięku osierdziowego., Ten początkowy problem został przypisany krzywej uczenia się operatora: przy doświadczeniu operatora wskaźnik powikłań spadł, a odsetek udanych implantacji znacznie się poprawił. Obecnie (w przypadku obu urządzeń) ponad 95% implantacji jest na ogół udanych, a wskaźnik ciężkiego wysięku osierdziowego jest
względy techniczne
technika okluzji przezskórnej LAA wymaga zespołu z doświadczeniem w chorobie wrodzonej / strukturalnej., Chociaż niektóre grupy używają tylko echokardiografii wewnątrzczołowej, lub nawet angiograficznej kontroli, do prowadzenia procedury i uniknąć intubacji pacjenta, większość ośrodków używać echokardiografii przełyku (TEE) w znieczuleniu ogólnym. Strukturalnie LAA ma bardzo cienkie ściany i heterogeniczną morfologię, która może ukryć mikrotrombozy z TEE. Doświadczenie operatora jest niezbędne, aby zminimalizować manipulację w LAA, a tym samym zmniejszyć ryzyko perforacji i zatoru okołoprocesowego., Dwa z najważniejszych czynników, które minimalizują manipulację w LAA są następujące: A) niskie tylne przebicie transseptalne, które ułatwia przednie podejście do LAA, oraz b) szczegółowe badanie LAA, jeśli to możliwe z tee i angiografii, w celu ustalenia morfologii LAA i uzyskania dokładnych pomiarów ułatwiających wybór wielkości okludery. Zaleca się wykonywanie pomiarów przy prawidłowej objętości krwi, ponieważ wielkość LAA może się znacznie różnić w zależności od poziomu nawodnienia pacjenta., W trakcie zabiegu pacjenci mają tendencję do odwodnienia, dlatego zaleca się oznaczenie ciśnienia w lewym przedsionku i podanie płynu w celu utrzymania ciśnienia >10 mmHg przed wykonaniem pomiarów.
jest to stosunkowo nowa procedura i mimo, że tee jest standardem obrazowania, idealny tryb obrazowania pozostaje nieznany. Morfologia LAA jest owalna u 80% chorych, więc średnice zwykle różnią się ze względu na krótkie i długie osie. Ta różnica może pozostać niezauważona z 2-wymiarowymi technikami obrazowania., Podobnie jak w procedurach takich jak przezskórna wymiana zastawki aortalnej, trójwymiarowa TEE lub tomografia serca może dostarczyć informacji przestrzennych, które mogą pomóc zoptymalizować strategię implantacji i wybór rozmiaru urządzenia.
znaczenie przecieków peryprotetycznych podczas obserwacji pozostaje niepewne. Subanaliza badania PROTECT Af nie wykazała związku między wyciekami a pojawieniem się zdarzeń klinicznych., Natomiast w badaniach wyników operacji serca wieńcowego, niepełne wycięcie LAA u pacjentów z chirurgiczną profilaktyczną niedrożnością LAA wiązało się z większym odsetkiem zdarzeń kardioembolicznych. Ponieważ czekamy na nowe badania, które mogą lub nie potwierdzą tego związku, powinniśmy starać się zapobiegać wyciekom periprotetycznym. Dlatego zaleca się, aby urządzenie było nieco większe niż sugerowałyby tee i środki angiograficzne, ponieważ umożliwia to zmniejszenie szybkości wycieków resztkowych bez zwiększania ryzyka pęknięcia ściany LAA.,13
Postprocesorowe zalecenia przeciwzakrzepowe to kolejny kontrowersyjny problem. W badaniu PROTECT AF, OAC podawano przez 45 dni po implantacji i zawieszano, jeśli tee wykazało odpowiednią niedrożność LAA.Ostatnio badanie ASAP wykazało, że 45-dniowe leczenie OAC może zastąpić podwójne leczenie przeciwpłytkowe (100 mg/dobę kwasu acetylosalicylowego i 75 mg/dobę klopidogrelu).Obecnie większość ośrodków zaleca podwójne leki przeciwpłytkowe przez 1 do 3 miesięcy i bezterminową monoterapię przeciwpłytkową., Zakrzepica urządzenia jest rzadkim powikłaniem, ale została opisana zarówno w urządzeniach Watchman™, jak i ACP. Chociaż powikłanie to ustępuje po 2 tygodniach leczenia przeciwzakrzepowego u większości pacjentów, potencjalne ryzyko zatoru z powodu migracji skrzepliny sprawia, że jest to jedno z najbardziej obawiających się powikłań., W jedynej zgłoszonej serii Hiszpańskiej alarmujący odsetek zakrzepicy urządzenia zaobserwowano u 14% pacjentów, w przeciwieństwie do 15 ta różnica w odsetku zakrzepicy może być spowodowana różnicą w czułości wykrywania: w rejestrze hiszpańskim protokół obserwacji tee był znacznie dłuższy (24 h i 1, 3, 6 i 12 miesięcy) niż w większości badanych ośrodków, w których tee był stosowany przez 3 do 6 miesięcy.,Biorąc pod uwagę, że większość przypadków zakrzepicy występowała po = 3 miesiącach, a wszystkie ustąpiły po podaniu heparyny sodowej lub enoksaparyny przez 2 tygodnie, określenie wykonalności 3-miesięcznego leczenia przeciwzakrzepowego lub bardziej wyczerpującej obserwacji może być rozwiązaniem w przyszłości, po wyjaśnieniu prawdziwej częstości występowania zakrzepicy narządu. W każdym przypadku konieczna jest wielodyscyplinarna, zindywidualizowana ocena u pacjentów tego typu, którzy czasami wykazują tak wysokie ryzyko krwawienia, że nawet krótkie okresy leczenia przeciwzakrzepowego mogą być przeciwwskazane.,
wnioski i perspektywy na przyszłość
chociaż NVAF jest już jedną z najczęstszych chorób w naszym społeczeństwie, jego częstość występowania wzrośnie w nadchodzących latach ze względu na postępujące starzenie się populacji. Z różnych powodów od 30% do 50% pacjentów wskazanych do OAC nie przyjmuje ich. Obecnie Laa occlusion stanowi alternatywę dla pacjentów z NVAF i przeciwwskazaniami do leczenia przeciwzakrzepowego., Laa occlusion jest skutecznym i bezpiecznym zabiegiem, ale wymaga zespołu z doświadczeniem w kardiologii interwencyjnej strukturalnej i wiąże się z istotną krzywą uczenia się dla operatora.
w przyszłości okluzja LAA może być alternatywą dla leczenia OAC dla wszystkich pacjentów z NVAF. Chociaż badanie PROTECT AF udowodniło już, że skuteczność okluzji LAA jest nie mniejsza niż w terapii przeciwzakrzepowej, początkowa krzywa uczenia warunkowała wysoki wskaźnik powikłań okołoprocesowych., Dwa nowe randomizowane badania-PREVAIL i ACP-porównają w szczególności okluzję LAA z leczeniem OAC u pacjentów z NVAF po pokonaniu początkowej krzywej uczenia się procedury. Badanie PREVAIL porównuje urządzenie Watchman™ z warfaryną, a ACP porównuje urządzenie ACP z warfaryną i dabigatranem. Jeśli wyniki obu badań wykażą, że okluzja LAA jest nie mniej skuteczna niż leczenie przeciwzakrzepowe u pacjentów z NVAF, stosowanie procedury może zostać przedłużone i może stać się alternatywą dla leczenia przeciwzakrzepowego u pacjentów o niższym profilu ryzyka.,
Xavier Freixa jest prorektorem St.Jude Medical.