en chimie, un énantiomère (/ˈˈnæntiəmər, ɛ-, -tioʊ-/ə-NAN-tee -ə-Mər; du Grec enνάντιος (enántios) « opposé », et μέρος (méros) « partie ») (également appelé isomère optique, antipode ou antipode optique) est l’un des deux stéréoisomères qui sont des images miroirs l’un de l’autre qui ne sont pas superposables (pas identiques), beaucoup comme les mains gauche et droite sont des images miroir l’une de l’autre qui ne peuvent pas apparaître identiques simplement par réorientation., Un seul atome chiral ou une caractéristique structurelle similaire dans un composé fait que ce composé a deux structures possibles qui ne sont pas superposables, chacune étant une image miroir de l’autre. Chaque membre de la paire est appelé énantiomorphe (enantio = opposé; morph = forme); la propriété structurelle est appelée énantiomérie. La présence de plusieurs caractéristiques chirales dans un composé donné augmente le nombre de formes géométriques possibles, bien qu’il puisse encore y avoir des paires parfait-miroir-image.,
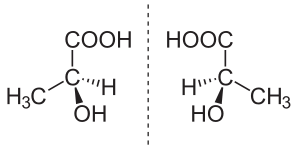
un échantillon d’un produit chimique est considéré comme énantiopure (également appelé énantiomériquement pur) lorsqu’il contient, dans les limites de détection, des molécules d’une seule chiralité.,
lorsqu’ils sont présents dans un environnement symétrique, les énantiomères ont des propriétés chimiques et physiques identiques, à l’exception de leur capacité à faire pivoter la lumière polarisée plane ( + / -) en quantités égales mais dans des directions opposées (bien que la lumière polarisée puisse être considérée comme un milieu asymétrique). De tels composés sont donc décrits comme optiquement actifs, avec des termes spécifiques pour chaque énantiomère en fonction de la direction: un composé dextrorotatoire fait tourner la lumière dans le sens horaire ( + ) tandis qu’un composé lévorotatoire fait tourner la lumière dans le sens antihoraire ( -)., Un mélange d’un nombre égal de deux énantiomères est appelé un mélange racémique ou un racémate. Dans un mélange racémique, la quantité de rotation positive est exactement contrecarrée par la quantité égale de rotation négative, de sorte que la rotation nette est nulle (le mélange n’est pas optiquement actif). À toutes fins utiles, les paires d’énantiomères ont la même énergie libre de Gibbs., Cependant, la physique théorique prédit qu’en raison de la violation de parité de la force nucléaire faible (la seule force dans la nature qui peut « dire de gauche à droite »), il y a en fait une différence d’énergie infime entre les énantiomères (de l’ordre de 10-12 eV ou 10-10 kJ/mol ou moins) en raison du faible mécanisme Cette différence d’énergie est beaucoup plus petite que les changements d’énergie causés par un changement même trivial de la conformation moléculaire et beaucoup trop petite pour être mesurée par la technologie actuelle, et est donc chimiquement sans conséquence.,
Les membres énantiomères ont souvent des réactions chimiques différentes avec d’autres substances énantiomères. Étant donné que de nombreuses molécules biologiques sont des énantiomères, il existe parfois une différence marquée dans les effets de deux énantiomères sur les organismes biologiques. Dans les médicaments, par exemple, souvent, un seul des énantiomères d’un médicament est responsable des effets physiologiques souhaités, tandis que l’autre énantiomère est moins actif, inactif ou parfois même productif d’effets indésirables., Grâce à cette découverte, des médicaments composés d’un seul énantiomère (« enantiopure ») peuvent être développés pour améliorer le fonctionnement du médicament et parfois éliminer certains effets secondaires. Un exemple est l’eszopiclone (Lunesta), qui n’est qu’un énantiomère unique d’un médicament racémique plus ancien appelé zopiclone. Un énantiomère est responsable de tous les effets souhaités, tandis que l’autre énantiomère semble être inactif, de sorte que la dose d’eszopiclone est la moitié de celle de zopiclone.
dans la synthèse chimique de substances énantiomères, les précurseurs Non énantiomères produisent inévitablement des mélanges racémiques., En l’absence d’un environnement énantiomérique efficace (précurseur, catalyseur chiral ou résolution cinétique), la séparation d’un mélange racémique en ses composants énantiomères est impossible, bien que certains mélanges racémiques cristallisent spontanément sous la forme d’un conglomérat racémique, dans lequel les cristaux des énantiomères sont physiquement séparés et peuvent être séparés mécaniquement (par exemple, les énantiomères de l’acide tartrique, dont les énantiomères cristallisés ont été séparés avec une pince À Épiler par Pasteur)., Cependant, la plupart des racémates cristalliseront dans des cristaux contenant les deux énantiomères dans un rapport de 1:1, disposés dans un réseau régulier.