kemian, yksi enantiomeeri (/ɪˈnæntiəmər, ɛ-, -tioʊ-/ ə-NAN-t-paita-ə-mər; kreikan ἐνάντιος (enántios) ’vastapäätä’, ja μέρος (meros) ’osa’) (myös nimeltään optinen isomeeri, antipode, tai optinen antipode) on yksi kaksi stereo, jotka ovat peilikuvia toisilleen, että ovat ei-superposable (ei identtiset), paljon kuin yksi on vasen ja oikea kädet ovat peili kuvia toisilleen, että voi esiintyä samanlaisia yksinkertaisesti suunnata., Yksi kiraalinen atomi tai vastaavia rakenteellinen ominaisuus yhdiste aiheuttaa sen, että yhdiste on kaksi mahdollista rakenteita, jotka ovat ei-superposable, jokainen peilikuva muiden. Jokaista parin jäsentä kutsutaan enantiomorfiksi (enantio = vastakohta; morph = muoto); rakenteellista ominaisuutta kutsutaan enantiomeeriksi. Läsnäolo useita kiraaliset ominaisuudet tietyn yhdisteen lisää useita geometrisia muotoja mahdollista, mutta saattaa silti olla joitakin täydellinen-peili-kuva-paria.,
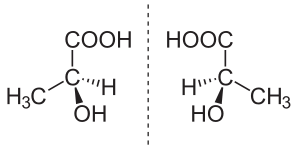
näytteen kemiallinen pidetään enantiopuhtaita (kutsutaan myös enantiomeerisesti puhtaita), kun se on rajoissa havaitseminen, molekyylit vain yksi kiraalisuus.,
Kun läsnä on symmetrinen ympäristö, enantiomeerit on samat kemialliset ja fysikaaliset ominaisuudet, lukuun ottamatta niiden kyky kiertää kone-polarisoitunut valo ( + / − ), jonka yhtä paljon mutta vastakkaisiin suuntiin (vaikka polarisoitunut valo voidaan pitää epäsymmetrisen medium). Tällaisia yhdisteitä ovat siis kuvata optisesti aktiivinen, kanssa erityiset ehdot kunkin enantiomeeri, joka perustuu suuntaan: dextrorotatory yhdiste kiertää valoa myötäpäivään ( + ) – suuntaan, kun taas levorotatory yhdiste kiertää valoa vastapäivään (–) suuntaan., Seosta yhtä paljon molempia enantiomeereja on niin sanottu raseeminen seos, tai rasemaatti. On raseeminen seos, määrä positiivinen kierto on täsmälleen torjua yhtä suuri määrä negatiivinen kierto, joten net kierto on nolla (seos ei ole optisesti aktiivinen). Kaikissa tarkoituksissa ja tarkoituksissa enantiomeerien pareilla on sama Gibbsin vapaa energia., Kuitenkin, teoreettinen fysiikka ennustaa, että koska pariteetti rikkoo heikko ydinvoima voima (ainoa voima luonnossa joka voi ”kertoa vasen oikealta”), on itse asiassa minuutin ero energian välillä enantiomeerit (suuruusluokkaa 10-12 eV tai 10-10 kJ/mol tai vähemmän), koska heikko neutraali nykyinen mekanismi. Tämä ero energia on paljon pienempi kuin energian aiheuttamia muutoksia jopa triviaali muutos, molekyylien rakenne ja liian pieni toimenpide, jonka nykyinen teknologia, ja on siksi kemiallisesti merkityksetön.,
Enantiomeeri jäsenillä on usein erilaisia kemiallisia reaktioita muiden enantiomeeri aineita. Koska monet biologiset molekyylit ovat enantiomeerit, siellä on joskus merkittävä ero vaikutukset kahden enantiomeerin biologisten organismien. Huumeita, esimerkiksi, usein vain yksi lääke, on enantiomeerit on vastuussa haluamasi fysiologisia vaikutuksia, kun taas toinen enantiomeeri on vähemmän aktiivinen, passiivinen, tai joskus jopa tuottava haittavaikutuksia., Koska tämä löytö, huumeet, joka koostuu vain yksi enantiomeeri (”enantiopuhtaita”) voidaan kehittää, jotta lääke toimisi paremmin ja joskus poistaa joitakin sivuvaikutuksia. Esimerkki on eszopiclone (Lunesta), joka on vain yksi enantiomeeri vanhempi raseeminen lääke, nimeltään zopiclone. Yksi enantiomeeri on vastuussa kaikista toivottuja vaikutuksia, kun taas toinen enantiomeeri näyttää olevan käytössä, joten annos eszopiclone on puolet zopiclone.
enantiomeeristen aineiden kemiallisessa synteesissä muut kuin enantiomeeriset lähtöaineet tuottavat väistämättä raseemisia seoksia., Ilman tehokasta enantiomeric ympäristö (esiaste, kiraalinen katalysaattori, tai kineettinen resoluutio), erottaminen raseeminen seos sen enantiomeric osia on mahdotonta, vaikka tietyt raseeminen seokset kiteytyä spontaanisti muodossa raseeminen monialayritys, jossa kiteitä enantiomeerit ovat fyysisesti erillään ja voidaan erottaa mekaanisesti (esim. enantiomeerit viinihapon, jonka kiteytynyt enantiomeerit erotettiin pinseteillä, jonka Pasteur)., Useimmat rasemaatit kuitenkin kiteytyvät kiteisiin, jotka sisältävät molemmat enantiomeerit 1: 1-suhteessa, joka on järjestetty säännölliseen hilaan.