On olemassa neljä lakia, jotka tunnetaan nimellä Kaasu Lait, jotka kuvaavat, miten kaasut käyttäytyvät. Neljä lakia ovat Boylen Laki, Charlesin Laki, Gay-Lussacin Laki ja Avogadron Laki.
Charlesin Laki
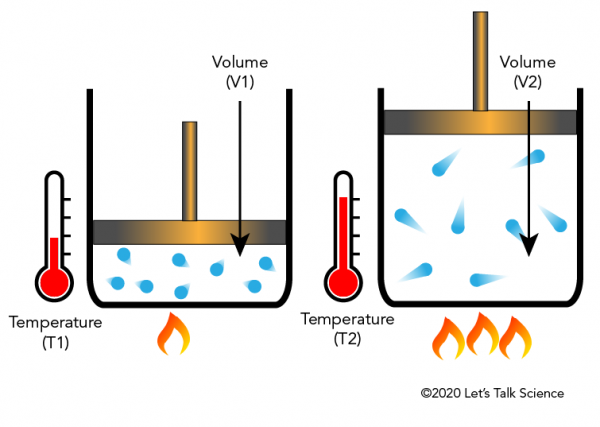
Jacques Charles, ranskan fyysikko, löydettiin vuonna 1780, että lämmitys kaasu, aiheuttaa se laajentaa tietty murto-osa. Alla oleva kuva näyttää, miten lämpö tekee molekyylit liikkuvat nopeammin ja osui puolin ja kansi, jossa on enemmän voimaa, mikä liikkuu kansi kiinni kun kaasu laajenee.,
Charlesin Laki Jokapäiväisessä Elämässä
jotta kuumailmapallo nousu, lämpöä lisätään ilmaa sisällä ilmapallo. Lämmön lisääminen saa molekyylit siirtymään kauemmas toisistaan.

arkikielessä voimme sanoa, että ilma sen sisällä laajenee. Tällöin ilmapallon ja sen sisällä olevan ilman kokonaistiheys (massa tilavuusyksikköä kohti) pienenee. Kun ilmapallon tiheys pienenee ulkoilman tiheyttä pienemmäksi, ilmapallo nousee. Vastaavasti kaasun tilavuus kutistuu, jos sen lämpötila laskee.
alla näkyy nestemäisen typen kaataminen vihreän ilmapallon päälle. Kylmä nestemäinen typpi jäähdyttää ilmaa ilmapallon sisällä., Tämän seurauksena ilman molekyylit hidastuvat aiheuttaen ilmapallon tilavuuden pienenemisen.

lomien Aikana, joku, jonka tunnet on käytetty turkki lämpömittari. Kalkkunalämpömittari juuttuu kalkkunaan keittäessään ja ponnahtaa sitten esiin, kun liha on tarpeeksi kypsää. Miten tämä ihmeellinen teknologia toimii? Se liittyy tietenkin Charlesin lakiin!, Kalkkunan lämpömittarin sisällä on pieni määrä ilmaa. Kun lämpötila nousee Turkin sisällä, ilma Turkin lämpömittarin sisällä laajenee. Kun se saavuttaa tietyn määrän, top ponnahtaa ja kertoo kokille, että kalkkuna on kunnolla keitetty.

Gay-Lussacin Laki
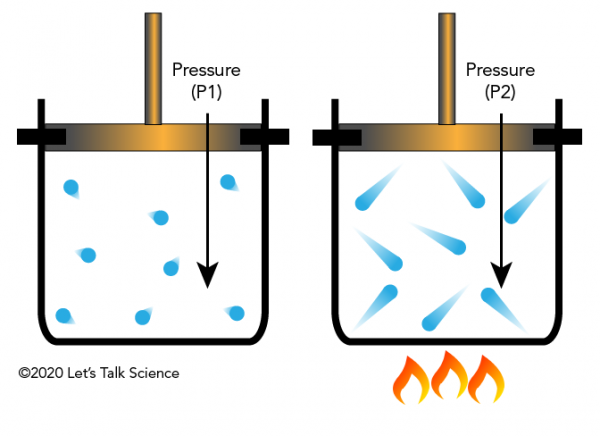
Joseph Louis Gay-Lussac oli ranskalainen kemisti ja fyysikko, joka löysi vuonna 1802, että jos pitää äänenvoimakkuutta kaasuvakio (kuten suljetussa astiassa), ja soveltaa lämmön, kaasun paine kasvaa. Tämä johtuu siitä, että kaasuilla on enemmän liike-energiaa, jolloin ne osuvat säiliön seinämiin enemmän voimaa (mikä johtaa suurempaan paineeseen).
Gay-Lussacin Laki Jokapäiväisessä Elämässä
Sisällä painekattila ruokaa, että haluat kokki istuu vedessä. Nestemäisen veden lämpötilan noustessa syntyy vesihöyryä (vettä sen kaasutilassa). Tämä höyry ei pääse karkuun painekattilasta – eli tilavuus ei muutu. Veden paine höyry nousee, kunnes veden lämpötila ja vesihöyryn ylittää normaalin veden kiehumispisteen (100 °C). Tässä korkeammassa lämpötilassa ruoka voidaan keittää paljon nopeammin., Sitkeä liha tulee myös paljon mureammaksi sen jälkeen, kun se on keitetty painekattilassa.

tiesitkö, että ilmanpaine sisällä auton renkaat muutoksia, kun auto on ajettu? Ajon jälkeen Ilmanpaine auton renkaissa nousee. Tämä johtuu siitä, että renkaiden ja tien välinen kitka (kosketusvoima) saa renkaiden sisällä olevan ilman lämpenemään., Ilman ei voi laajentaa, koska renkaat ovat pääasiallisesti kiinteän tilavuuden säiliö, niin paine kasvaa – tämä on Gay-Lussacin Laki!