Heterogeeninen Katalyysi
heterogeeninen katalyysi, katalysaattori on eri vaiheessa reagenssit. Ainakin yksi reagenssit vuorovaikutuksessa kiinteä pinta on fyysinen prosessi, jota kutsutaan adsorptio siten, että kemiallinen sidos lähtöaineen tulee heikko ja sitten taukoja. Myrkyt ovat aineita, jotka sitoutuvat peruuttamattomasti katalyytteihin estäen reaktanttien adsorboitumista ja siten vähentävät tai tuhoavat katalyytin tehokkuutta.,
esimerkki heterogeeninen katalyysi on vuorovaikutus vetykaasun kanssa metallin pinnan, kuten Ni, Pd, tai Pt. Kuten kuvassa \(\PageIndex{2}\) olevassa A osassa esitetään, vety-vetysidokset hajoavat ja tuottavat yksittäisiä adsorboituneita vetyatomeja metallin pinnalle. Koska adsorboitu atomit voivat liikkua pinnalla, kaksi vety atomia voivat törmäävät ja muodostavat molekyylin vety-kaasua, joka voi sitten jättää pinnan käänteinen prosessi, jota kutsutaan desorptio. Metallipinnan adsorboituneet h-atomit ovat huomattavasti reaktiivisempia kuin vetymolekyyli., Koska suhteellisen vahva H–H-sidoksen (dissosiaatio energia = 432 kJ/mol) on jo rikki, energia este useimmille reaktioita H2 on huomattavasti pienempi katalyytin pinnalle.
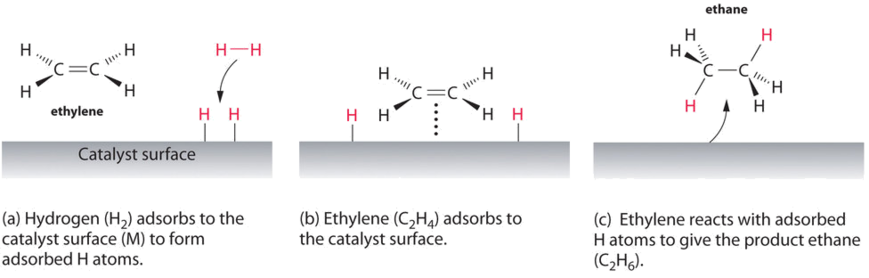
Kuva \(\PageIndex{2}\) osoittaa, prosessi nimeltä hydraus, jossa vetyatomit lisätään kaksoissidos on alkeeni, kuten eteenin, antaa tuote, joka sisältää C–C yhden joukkovelkakirjat, tässä tapauksessa etaania., Hydraus on käytetty elintarviketeollisuudessa muuntaa kasviöljyt, joka koostuu pitkistä ketjuista, alkeenit, enemmän kaupallisesti arvokas kiinteä johdannaiset, jotka sisältävät alkyyli-ketjut. Joidenkin monityydyttymättömien kasviöljyjen kaksoissidosten hydraus tuottaa esimerkiksi margariinia, tuotetta, jonka sulamispiste, rakenne ja muut fysikaaliset ominaisuudet muistuttavat voin ominaisuuksia.
useita tärkeitä esimerkkejä teollisuuden heterogeenisistä katalyyttisistä reaktioista on taulukossa \(\PageIndex{1}\)., Vaikka mekanismit, joilla nämä reaktiot ovat huomattavasti monimutkaisempia kuin yksinkertainen hydraus reaktio kuvattu täällä, ne kaikki liittyy adsorptio reagenssit päälle vankka katalyyttinen pinta, kemiallinen reaktio adsorboitu lajit (joskus kautta useita väli-lajit), ja lopuksi desorptio tuotteiden pinnalta.