Glykosidische Bindungsbildung
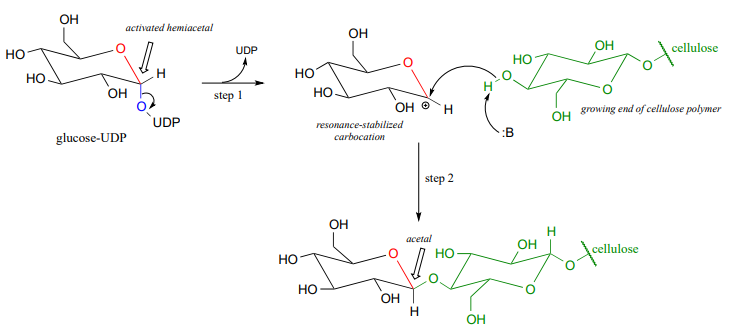
Betrachten wir nun die Acetalbildung in einem biochemischen Kontext. Ein sehr wichtiges Beispiel für die Acetal / Ketal-Gruppe in der Biochemie sind die glykosidischen Bindungen, die einzelne Zuckermonomere zu Polysacchariden verbinden (siehe Abschnitt 1.3 für einen schnellen Überblick)., Schauen Sie sich die glykosidische Bindung zwischen zwei Glukosemonomeren in einer Cellulasekette an:
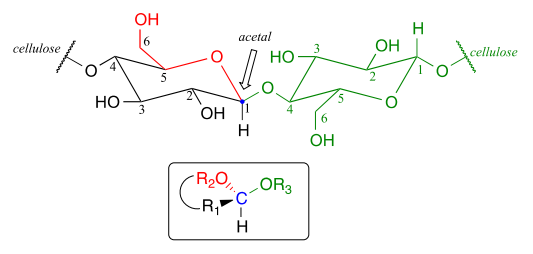
Wenn Sie genau hinschauen, sollten Sie erkennen, dass Kohlenstoff #1, der anomere Kohlenstoff auf dem linken Glukosemonomer, der zentrale Kohlenstoff einer Acetalgruppe ist. Biochemiker bezeichnen dies als b-1,4-Verknüpfung, da die Stereochemie bei Kohlenstoff #1 im spezialisierten Kohlenhydrat-Nomenklatursystem b ist und mit Kohlenstoff #4 der nächsten Glukose in der Kette verbunden ist., Die große strukturelle Vielfalt der Kohlenhydrate beruht zum großen Teil auf den verschiedenen möglichen Verbindungen-sowohl in Bezug auf die zwei Kohlenstoffverbindungen als auch auf die Stereochemie der Verknüpfung. Wenn Sie die Kohlenhydratbiochemie genauer untersuchen, werden Sie viele weitere Variationen der glykosidischen Bindungs-Verknüpfungsmuster sehen.,
Reaktionen, bei denen neue glykosidische Bindungen gebildet werden, werden durch Enzyme, sogenannte Glykosyltransferasen, katalysiert, und in organischer Chemie stellen diese Reaktionen die Umwandlung eines Hemiacetals in ein Acetal dar (denken Sie daran, dass Zuckermonomere in ihrer zyklischen Form Hemiacetale und Hemiketale sind)., Der Mechanismus der Glykosidenbindungsbildung in einer lebenden Zelle verläuft parallel zum säurekatalysierten(nicht biologischen) acetalbildenden Mechanismus mit einem wichtigen Unterschied: Anstatt protoniert zu werden, wird die \(OH\) Gruppe des Hemiacetals durch Phosphorylierung in eine gute Zellgruppe umgewandelt (dies ist ein Muster, mit dem wir aus den Kapiteln 9 und 10 vertraut sind). Die spezifische Identität der aktivierenden Phosphatgruppe variiert für verschiedene Reaktionen, so dass sie in der folgenden Abbildung verallgemeinert wird.,
Mechanismus zur (biochemischen) Acetalbildung:
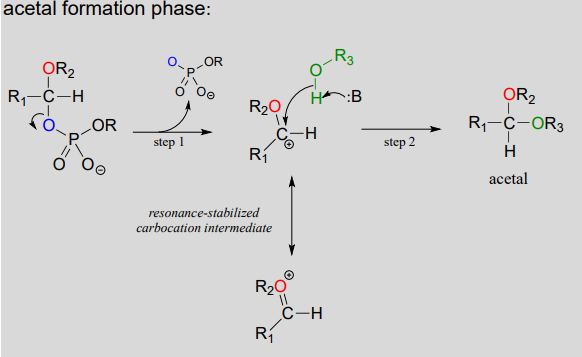
- Schritt A (Aktivierungsphase): Diese Phase der Reaktion variiert je nach Einzelfall, beinhaltet jedoch immer die Gruppenübertragungsschritte, die aus Kapitel 9 bekannt sind. Was für unsere gegenwärtige Diskussion jedoch am wichtigsten ist, ist einfach, dass die Hydroxylgruppe auf dem Hemiacetal aktiviert wurde-dh. zu einer guten Gruppe gemacht – durch Phosphorylierung.,
- Schritt 1: Nachdem die Leaving-Gruppe aktiviert wurde, erledigt sie ihre Aufgabe und verlässt, was zu einer resonanzstabilisierten Carbocation führt.
- Schritt 2: Ein nukleophiler Alkohol an der wachsenden Cellulosekette greift die hochelektrophile Carbokation zu einem Acetal an. Hier wird die Stereochemie der neuen glykosidischen Bindung bestimmt: Abhängig von der Reaktion könnte sich das Alkoholnukleophile von beiden Seiten der planaren Carbokation nähern.,
Um es noch einmal zu wiederholen: Es ist wichtig, das bekannte \(S_N1\) mechanistische Muster zu erkennen, das hier im Spiel ist: In Schritt A wird eine schlechte Abgangsgruppe in eine gute Abgangsgruppe umgewandelt, in Schritt 1 verlässt die Abgangsgruppe und eine stabilisierte Carbokation wird zurückgelassen, und in Schritt 2 greift ein nucleophile an, um eine neue Bindung zu bilden und den Substitutionsprozess abzuschließen. Schauen Sie zurück auf die\ (S_N1\) Reaktionen, die wir in Kapitel 8 gesehen haben, wenn Sie Probleme haben, diese mechanistische Verbindung herzustellen.,
Schauen wir uns nun speziell den Glykosyltransferase-Reaktionsmechanismus an, bei dem eine neue glykosidische Bindung an einer wachsenden Cellulosekette gebildet wird. Glukose (ein Hemiacetal) wird zuerst durch zwei enzymatische Phosphatübertragungsschritte aktiviert: Schritt A1, eine Phosphatisomerisierungsreaktion mit einem Mechanismus ähnlich der Reaktion in Problem P9.13, gefolgt von einem phosphatisationsabhängigen Schritt A2, für den Sie aufgefordert wurden, einen Mechanismus in Problem P9.12 vorzuschlagen.,
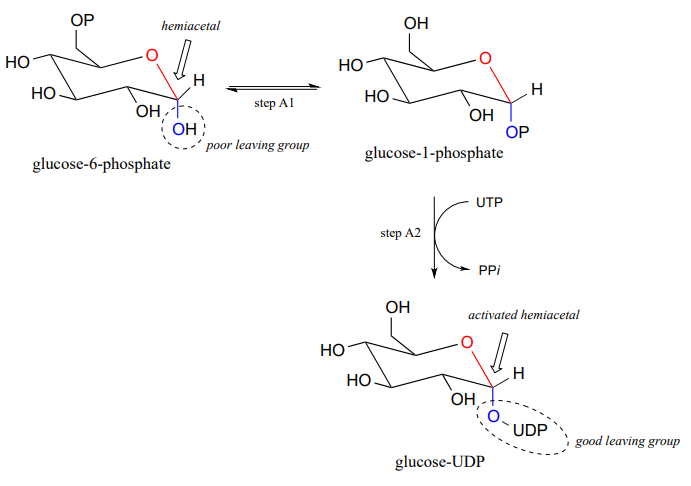
Die UDP-Gruppe auf Glucose-UDP verlässt dann (Schritt 1 unten) und bildet ein resonanzstabilisiertes Carbokationszwischenprodukt. Der Angriff der Alkoholgruppe auf die wachsende Cellulosekette in Schritt 2 bildet die glykosidische (acetale) Bindung. Beachten Sie die Inversion der Stereochemie.